题目内容
次磷酸钠(NaH2PO2)是唯一的次磷酸的钠盐(不存在酸式盐).下列叙述中正确的是( )
| A、次磷酸(H3PO2)是三元酸 |
| B、H3PO2中磷为+1价 |
| C、NaH2PO2溶液呈酸性 |
| D、次磷酸根离子为-3价 |
考点:氮族元素简介
专题:元素及其化合物
分析:A、根据次磷酸的钠盐不存在酸式盐来判断是几元酸;
B、根据化合价规则确定P元素的化合价;
C、根据次磷酸不存在酸式盐来回答;
D、根据NaH2PO2中钠元素是+1价,结合化合价规则来确定次磷酸根离子的价态.
B、根据化合价规则确定P元素的化合价;
C、根据次磷酸不存在酸式盐来回答;
D、根据NaH2PO2中钠元素是+1价,结合化合价规则来确定次磷酸根离子的价态.
解答:
解:次磷酸钠(NaH2PO2)是唯一的次磷酸的钠盐,不存在酸式盐,次磷酸(H3PO2)是一元酸,故A错误;
B、H3PO2中H为+1价,O为-2价,根据化合价规则,磷为+1价,故B正确;
C、次磷酸不存在酸式盐,所以NaH2PO2溶液中的阴离子水解导致溶液呈碱性,故C错误;
D、NaH2PO2中钠元素是+1价,次磷酸根离子为-1价,故D错误.
故选B.
B、H3PO2中H为+1价,O为-2价,根据化合价规则,磷为+1价,故B正确;
C、次磷酸不存在酸式盐,所以NaH2PO2溶液中的阴离子水解导致溶液呈碱性,故C错误;
D、NaH2PO2中钠元素是+1价,次磷酸根离子为-1价,故D错误.
故选B.
点评:本题考查学生元素的化合价的判断、化合价规则的使用以及元素以及化合物的性质知识,注意知识的迁移和应用是关键,难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
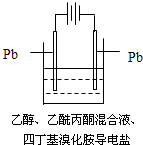 有机电解制备的金属醇盐,可直接作为制备纳米材料的前体.以下是一种电化学合成金属醇盐的主要装置.在电解过程中,已知乙醇和乙酰丙酮(CH3COCH2COCH3)在阴极发生的电极反应为:
有机电解制备的金属醇盐,可直接作为制备纳米材料的前体.以下是一种电化学合成金属醇盐的主要装置.在电解过程中,已知乙醇和乙酰丙酮(CH3COCH2COCH3)在阴极发生的电极反应为:2CH3CH2OH+2e-=2CH3CH2O-+H2↑
2CH3COCH2COCH3+2e-=2(CH3COCHCOCH3)+H2↑
下列说法正确的是( )
| A、阳极Pb失去电子,发生还原反应 |
| B、当阳极失去2 mol e-时,阴极产生2 mol氢气 |
| C、电解过程中,阳离子向阴极移动 |
| D、已知Pb-4e-=Pb4+,当消耗Pb的质量为103.5 g时,则转移电子2 mol |
下列物质的名称分别是试综合上述命名规律,分析思考后回答K2CS3的名称是( )
| 名称 | 硫代硫酸钠 | 多硫化钙 | 过氧化钡 | 超氧化钾 |
| 化学式 | Na2S2O3 | CaSx | BaO2 | KO2 |
| A、三硫代碳酸钾 |
| B、多硫代碳酸钾 |
| C、过硫碳酸钾 |
| D、超硫代碳酸钾 |
用NA表示阿伏加德罗常数,下列说法正确的是( )
| A、18g D2O含有的电子数为10NA |
| B、1mol Na2O2与水完全反应时转移电子数为2NA |
| C、12g石墨烯(单层石墨)中含有六元环的个数为0.5NA |
| D、200mL1mol/LFe2(SO4)3溶液中,Fe3+和SO42-离子数的总和是NA |
某同学用如图装置研究电化学实验,下列叙述正确的是( )
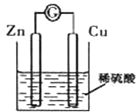

| A、铜为负极,产生气泡 |
| B、溶液变蓝色 |
| C、电子从锌极经导线流向铜极 |
| D、Zn、Cu 分别接外加电源的正、负极可在锌极镀上铜 |
下列有关化学基本概念的判断不正确的是( )
①溶液与胶体的本质区别是能否发生丁达尔效应
②根据是否仅含一种元素分为纯净物与混合物
③氧化还原反应的本质是反应前后元素化合价变化
④强电解质与弱电解质本质区别水溶液中导电性强弱
⑤根据酸分子中含有的H原子个数将酸分为一元酸、二元酸、多元酸
⑥MgO、Na2O2、CuO、Al2O3都是金属氧化物,也是碱性氧化物.
①溶液与胶体的本质区别是能否发生丁达尔效应
②根据是否仅含一种元素分为纯净物与混合物
③氧化还原反应的本质是反应前后元素化合价变化
④强电解质与弱电解质本质区别水溶液中导电性强弱
⑤根据酸分子中含有的H原子个数将酸分为一元酸、二元酸、多元酸
⑥MgO、Na2O2、CuO、Al2O3都是金属氧化物,也是碱性氧化物.
| A、①②④ | B、③⑤⑥ |
| C、④⑤ | D、全部错误 |
运用相关化学知识进行判断,下列结论错误的是( )
| A、增大反应物浓度可加快反应速率,因此用浓硫酸与铁反应能增大生成H2的速率 |
| B、NH4F水溶液中含有HF,因此NH4F溶液不能存放于玻璃试剂瓶中 |
| C、可燃冰主要甲烷与水在低温高压下形成的水合物晶体,因此可存在于海底 |
| D、需要加热的反应不一定是吸热反应 |