题目内容
13.请根据所学知识回答下列问题:(1)同温同压下,反应H2(g)+Cl2(g)═2HCl(g)在光照和点燃条件下的△H(化学计量数相同)分别为△H1、△H2,△H1=△H2(填“>”“<”或“=”下同).
(2)相同条件下,2mol氢原子所具有的能量>1mol 氢分子所具有的能量.
(3)已知常温时红磷比白磷稳定,比较下列反应中△H的大小:△H1<△H2.
①P4(白磷,s)+5O2(g)═2P2O5(s)△H1
②4P(红磷,s)+5O2(g)═2P2O5(s)△H2
(4)已知:稀溶液中,H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ•mol-1,则浓硫酸与稀氢氧化钠溶液反应生成1mol水,放出的热量>57.3kJ.
(5)已知:0.5mol CH4(g)与0.5mol水蒸气在t℃、p kPa 时,完全反应生成CO和H2的混合气体,吸收了a kJ 热量,该反应的热化学方程式是CH4(g)+H2O(g)=CO(g)+3H2(g)△H=+2akJ/mol.
(6)已知:C3H8(g )═CH4(g)+HC≡CH(g)+H2(g)△H1=156.6kJ•mol-1
CH3CH=CH2(g)═CH4(g)+HC≡CH(g)△H2=32.4kJ•mol-1
则相同条件下,反应C3H8(g)═CH3CH=CH2 (g)+H2(g)的△H=+124.2kJ•mol-1.
分析 (1)反应热与反应条件无关;
(2)原子结合为分子会放出能量;
(3)常温时红磷比白磷稳定,说明白磷能量高,反应放出的热量较多;
(4)浓硫酸溶于水放热;
(5)根据热化学方程式的含义以及书写方法来回答,计算对应化学方程式计量数的反应焓变,标注物质聚集状态写出;
(6)依据热化学方程式和盖斯定律计算得到.
解答 解:(1)同温同压下,反应H2(g)+Cl2(g)═2HCl(g)在光照和点燃条件下的△H(化学计量数相同)分别为△H1、△H2,反应热与条件无关,反应热相同,则△H1=△H2,
故答案为:=;
(2)原子结合为分子会放出能量,则相同条件下,2mol氢原子所具有的能量>1mol 氢分子所具有的能量;
故答案为:>;
(3)常温时红磷比白磷稳定,说明白磷能量高,反应放出的热量较多,因△H<0,则放出的能量越多反应热越小,
故答案为:<;
(4)浓硫酸溶于水放热,所以浓硫酸与稀氢氧化钠溶液反应生成1mol水,放出的热量大于57.3kJ,
故答案为:>;
(5)甲烷和水蒸气之间的反应方程式为:CH4(g)+H2O(g)=CO(g)+3H2(g),0.5mol甲烷与0.5mol水蒸气在t℃、p kPa时,完全反应生成一氧化碳和氢气(合成气),吸收了akJ热量,所以1mol甲烷与1mol水蒸气在t℃、p kPa时,完全反应生成一氧化碳和氢气(合成气),吸收了akJ热量,热化学方程式为:CH4(g)+H2O(g)=CO(g)+3H2(g)△H=+2akJ/mol,
故答案为:CH4(g)+H2O(g)=CO(g)+3H2(g)△H=+2akJ/mol;
(6)①C3H8(g)→CH4(g)+HC≡CH(g)+H2(g)△H1=156.6kJ•mol-1
②CH3CH=CH2(g)→CH4(g)+HC≡CH(g)△H2=32.4kJ•mol-1
依据盖斯定律①-②得到C3H8(g)→CH3CH=CH2(g)+H2(g)△H=+124.2KJ/mol
则相同条件下,反应C3H8(g)→CH3CH=CH2(g)+H2(g)△H=+124.2KJ/mol;
故答案为:+124.2.
点评 本题考查了反应热的计算、热化学方程式和盖斯定律计算应用,注意把握反应热的计算方法、热化学方程式的书写方法以及盖斯定律的含义,掌握基础是关键,题目难度中等.

 发散思维新课堂系列答案
发散思维新课堂系列答案| A. | 25℃时,0.1mol•L-1HF 溶液中pH=1 | |
| B. | Ksp(CaF2)随温度和浓度的变化而变化 | |
| C. | 加入CaCl2溶液后体系中的c(H+)不变 | |
| D. | 该体系中HF与CaCl2反应产生沉淀 |
 已知:2CrO42-+2H+?Cr2O72-+H2O.25℃时,调节初始浓度为1.0mol•L-1 的Na2CrO4溶液的pH,测定平衡时溶液中c(Cr2O72-)和c(H+),获得如图所示的曲线.下列说法不正确的是( )
已知:2CrO42-+2H+?Cr2O72-+H2O.25℃时,调节初始浓度为1.0mol•L-1 的Na2CrO4溶液的pH,测定平衡时溶液中c(Cr2O72-)和c(H+),获得如图所示的曲线.下列说法不正确的是( )| A. | 平衡时,pH越小,c(Cr2O72-)越大 | |
| B. | A点CrO42-的平衡转化率为50% | |
| C. | A点CrO42-转化为Cr2O72-反应的平衡常数K=1014 | |
| D. | 平衡时,若溶液中c(Cr2O72-)=c(Cr2O42-),则c(H+)>2.0×10-7 mol•L-1 |
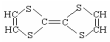 则该物质属于( )
则该物质属于( )| A. | 烯烃 | B. | 无机物 | C. | 有机物 | D. | 烷烃 |
