题目内容
10.现根据下列3个热化学反应方程式:Fe2O3(s)+3CO(g)═2Fe(s)+3CO2(g)△H=-25kJ/mol
3Fe2O3(s)+CO(g)═2Fe3O4(s)+CO2(g)△H=-47kJ/mol
FeO(s)+CO(g)═Fe(s)+CO2(g)△H=-11kJ/mol
写出CO气体还原Fe3O4固体得到FeO 固体和CO2气体的热化学反应方程式:Fe3O4(s)+CO(g)═3FeO+CO2(g)△H=+19kJ/mol.
分析 ①Fe2O3(s)+3CO(g)═2Fe(s)+3CO2(g)△H=-25kJ/mol
②3Fe2O3(s)+CO(g)═2Fe3O4(s)+CO2(g)△H=-47kJ/mol
③FeO(s)+CO(g)═Fe(s)+CO2(g)△H=-11kJ/mol
(①×3-②-③×6)×$\frac{1}{2}$得CO气体还原Fe3O4固体得到FeO 固体和CO2气体的热化学反应方程式.
解答 解:①Fe2O3(s)+3CO(g)═2Fe(s)+3CO2(g)△H=-25kJ/mol
②3Fe2O3(s)+CO(g)═2Fe3O4(s)+CO2(g)△H=-47kJ/mol
③FeO(s)+CO(g)═Fe(s)+CO2(g)△H=-11kJ/mol
(①×3-②-③×6)×$\frac{1}{2}$得CO气体还原Fe3O4固体得到FeO 固体和CO2气体的热化学反应方程式:Fe3O4(s)+CO(g)═3FeO+CO2(g)△H=+19 kJ/mol,
故答案为:Fe3O4(s)+CO(g)═3FeO+CO2(g)△H=+19 kJ/mol.
点评 本题考查反应热的计算,题目难度不大,注意盖斯定律的应用.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
1.(1)已知Na2S2O3+H2SO4=Na2SO4+S↓+SO2↑+H2O.甲同学通过测定该反应发生时溶液变浑浊的时间,研究外界条件对化学反应速率的影响.设计实验如下(所取溶液体积均为10mL):
其他条件不变时:探究温度对化学反应速率的影响,应选择①④(填实验编号);
探究浓度对化学反应速率的影响,应选择①②或③④(填实验编号);
(2)已知Na2S2O3溶液与Cl2反应时,1mol Na2S2O3转移8mol电子.该反应的离子方程式是5H2O+S2O32-+4Cl2=2SO42-+8Cl-+10H+.
| 实验编号 | 实验温度/℃ | c(Na2S2O3)/mol•L-1 | c(H2SO4)/mol•L-1 |
| ① | 25 | 0.1 | 0.1 |
| ② | 25 | 0.1 | 0.2 |
| ③ | 50 | 0.2 | 0.1 |
| ④ | 50 | 0.1 | 0.1 |
探究浓度对化学反应速率的影响,应选择①②或③④(填实验编号);
(2)已知Na2S2O3溶液与Cl2反应时,1mol Na2S2O3转移8mol电子.该反应的离子方程式是5H2O+S2O32-+4Cl2=2SO42-+8Cl-+10H+.
15.下列有机化合物的命名中正确的是( )
| A. | 1-甲基戊烷 | B. | 2-乙基戊烷 | ||
| C. | 2,5-二甲基己烷 | D. | 2,4,4-三甲基戊烷 |
2.下列有关说法不正确的是( )
| A. | 羊毛、棉花、淀粉都是自然界存在的天然高分子化合物 | |
| B. | 生物炼铜的原理是利用某些具有特殊本领的细菌把不溶性的硫化铜转化为铜离子 | |
| C. | 某反应的△H>0、△S<0,则该反应一定不能正向进行 | |
| D. | 为加快漂白精的漂白速率,使用时可滴加几滴醋酸 |
19.下列系统命名法正确的是( )
| A. | 4-乙基-2-戊烯 | B. | 3-甲基-3-戊醇 | ||
| C. | 2-甲基-1-戊炔 | D. | 2-甲基-3-乙基-2-丁醇 |
20.设NA为阿伏加德罗常数的数值.下列说法正确的是( )
| A. | 1 mol甲苯含有6NA个C-H键 | |
| B. | 5NH4NO3$\frac{\underline{\;\;△\;\;}}{\;}$2HNO3+4N2↑+9H2O的反应中,生成28 g N2,转移的电子数目为3.75NA | |
| C. | 标准状况下,22.4 L氨水含有NA个NH3分子 | |
| D. | 56 g铁片投入足量浓硫酸中生成NA个SO2分子 |
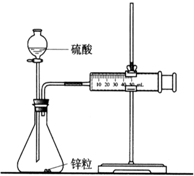 某化学兴趣小组的甲、乙两位同学对测定化学反应速率非常感兴趣,为此进行了有关的实验探究,实验记录如下.
某化学兴趣小组的甲、乙两位同学对测定化学反应速率非常感兴趣,为此进行了有关的实验探究,实验记录如下.