题目内容
 TiO2在光照下可使水分解:2H2O
TiO2在光照下可使水分解:2H2O
| ||
| 光 |
| A、该装置可以将光能转化为电能,同时电能转化为化学能 |
| B、铂电极上发生的反应为:2H++2e-=H2↑ |
| C、该装置工作时,电流由TiO2电极流向铂电极 |
| D、该装置工作时,TiO2电极附近溶液的pH变小 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:A、根据发生的反应及能量转化分析;
B、根据装置示意图可知铂电极上为氢离子得电子生成氢气;
C、氢氧根离子在TiO2电极上失电子,根据电子流向判断,电流流向;
D、TiO2电极附近为氢氧根离子反应.
B、根据装置示意图可知铂电极上为氢离子得电子生成氢气;
C、氢氧根离子在TiO2电极上失电子,根据电子流向判断,电流流向;
D、TiO2电极附近为氢氧根离子反应.
解答:
解:A、在光照下TiO2分解水,同时提供电能,所以该装置可以将光能转化为电能,同时电能转化为化学能,故A正确;
B、根据装置示意图可知铂电极上有氢气生成,则铂电极上为氢离子得电子生成氢气,所以铂电极上发生的反应为:2H++2e-=H2↑,故B正确;
C、氢氧根离子在TiO2电极上失电子,则电子从TiO2电极流向铂电极,所以电流铂电极流向TiO2电极,故C错误;
D、TiO2电极附近为为水中氢氧根离子失电子生成氢氧,同时生成氢离子,则TiO2电极附近溶液的pH变小,故D正确.
故选C.
B、根据装置示意图可知铂电极上有氢气生成,则铂电极上为氢离子得电子生成氢气,所以铂电极上发生的反应为:2H++2e-=H2↑,故B正确;
C、氢氧根离子在TiO2电极上失电子,则电子从TiO2电极流向铂电极,所以电流铂电极流向TiO2电极,故C错误;
D、TiO2电极附近为为水中氢氧根离子失电子生成氢氧,同时生成氢离子,则TiO2电极附近溶液的pH变小,故D正确.
故选C.
点评:本题考查了原电池原理的应用,注意根据两极发生的反应判断正负极及电子流向,题目难度中等.

练习册系列答案
相关题目
2014年,“安全”是人们关注的热点,以下做法能合理有效提高“食品安全”的是( )
| A、食品加工,禁止使用化学添加剂 |
| B、食品包装,用聚乳酸材料替代聚乙烯 |
| C、蔬菜种植,禁止使用化肥和农药 |
| D、饮水处理,用高铁酸钾替代氯气和明矾 |
利用下列实验方案可以从海洋动物柄海鞘中提取具有抗肿瘤作用的活性物质.下列说法错误的是( )


| A、步骤(1)需要过滤装置 |
| B、步骤(3)需要用到蒸发皿 |
| C、步骤(4)是利用物质的沸点差异进行分离的 |
| D、活性物质易溶于有机溶剂,难溶于水 |
化学式为C5H10O2的物质中,能与Na2CO3反应的放出气体的物质的结构共有( )
| A、2种 | B、3种 | C、4种 | D、5种 |
X、Y、Z、W、M五种元素的原子序数依次增大.已知X、Y、Z、W是短周期元素中的四种非金属元素,X元素的原子形成的离子就是一个质子;Y原子的最外层电子数是内层电子数的2倍;Z、W在元素周期表中处于相邻的位置,它们的单质在常温下均为无色气体;M是地壳中含量最高的金属元素.下列说法正确的是( )
| A、五种元素的原子半径从大到小的顺序是:M>W>Z>Y>X |
| B、X、Z两元素能形成原子个数比(X:Z)为3:1和4:2的化合物 |
| C、化合物YW2、ZW2都是酸性氧化物 |
| D、用M单质作阳极,石墨作阴极电解NaHCO3溶液,电解一段时间后,在阴极区会出现白色沉淀 |
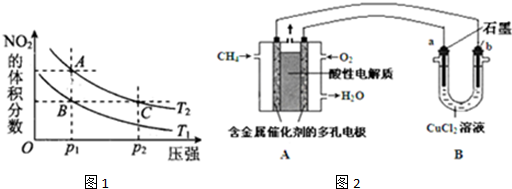
 工业上常产生大量的废气、废水、废渣、废热,如果处理不好,随意排放,会造成污染,而如果科学回收,可变废为宝.
工业上常产生大量的废气、废水、废渣、废热,如果处理不好,随意排放,会造成污染,而如果科学回收,可变废为宝.