题目内容
1.镁电池放电时电压高而平稳,镁电池成为人们研制的绿色电池,一种镁电池的反应式为xMg+Mo3S4$?_{充电}^{放电}$MgxMo3S4,下列说法中正确的是( )| A. | 充电时MgxMo3S4只发生还原反应 | |
| B. | 放电时Mo3S4只发生氧化反应 | |
| C. | 充电时阳极反应式为 Mo3S42x--2xe-=Mo3S4 | |
| D. | 放电时负极反应式为xMg=xMg2+-2xe- |
分析 由总反应式可知,放电时,为原电池反应,Mg化合价升高,被氧化,电极反应式为Mg-2e-=Mg2+,Mo3S4被还原,为原电池正极反应,电极反应式为Mo3S4+2xe-=Mo3S42x-,充电是电能转化为化学能的过程,阴极反应和原电池负极相反,阳极反应和原电池正极相反,以此解答该题.
解答 解:A.充电时,MgxMo3S4分别生成Mg和Mo3S4,发生氧化还原反应,故A错误;
B.放电时,负极上镁失电子发生氧化反应,Mo3S4发生还原反应,故B错误;
C.充电时,阳极反应和原电池正极相反,则阳极反应式:Mo3S42x--2xe-=Mo3S4,故C正确;
D.负极电极反应式为Mg-2e-=Mg2+,故D错误.
故选C.
点评 本题考查原电池与电解池知识,侧重于学生的分析能力的考查,题目难度中等,注意根据电池总反应书写电极反应式,此为解答该题的关键,学习中注意体会书写方法.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
12.利用下列装置(部分仪器已省略),能顺利完成对应实验的是( )
| A. | 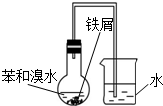 实验室制取溴苯 | B. | 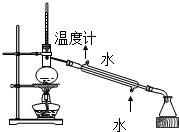 石油的分馏实验 | ||
| C. | 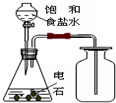 实验室制取乙炔并收集 | D. |  利用酒精萃取碘水中的I2单质 |
16.除去下列物质中的杂质(括号内为杂质),所选用的试剂不正确的一组是( )
| 选项 | 待提纯的物质 | 选用的试剂 |
| A | N2(O2) | 灼热的铜网 |
| B | SO2(SO3) | 饱和Na2SO3溶液 |
| C | H2(H2S) | CuSO4溶液 |
| D | CO2(SO2) | 酸性KMnO4溶液 |
| A. | A | B. | B | C. | C | D. | D |
6.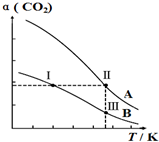 将燃煤废气中的CO2转化为二甲醚的反应原理为:2CO2(g)+6H2(g)$\stackrel{催化剂}{?}$CH3OCH3(g)+3H2O(g),一定条件下,现有两个体积均为1.0L恒容密闭容器甲和乙,在甲中充入0.1molCO2和0.2molH2,在乙中充入0.2molCO2和0.4molH2,发生上述反应并达到平衡.该反应中CO2的平衡转化率随温度的变化曲线如图所示.下列说法正确的是( )
将燃煤废气中的CO2转化为二甲醚的反应原理为:2CO2(g)+6H2(g)$\stackrel{催化剂}{?}$CH3OCH3(g)+3H2O(g),一定条件下,现有两个体积均为1.0L恒容密闭容器甲和乙,在甲中充入0.1molCO2和0.2molH2,在乙中充入0.2molCO2和0.4molH2,发生上述反应并达到平衡.该反应中CO2的平衡转化率随温度的变化曲线如图所示.下列说法正确的是( )
 将燃煤废气中的CO2转化为二甲醚的反应原理为:2CO2(g)+6H2(g)$\stackrel{催化剂}{?}$CH3OCH3(g)+3H2O(g),一定条件下,现有两个体积均为1.0L恒容密闭容器甲和乙,在甲中充入0.1molCO2和0.2molH2,在乙中充入0.2molCO2和0.4molH2,发生上述反应并达到平衡.该反应中CO2的平衡转化率随温度的变化曲线如图所示.下列说法正确的是( )
将燃煤废气中的CO2转化为二甲醚的反应原理为:2CO2(g)+6H2(g)$\stackrel{催化剂}{?}$CH3OCH3(g)+3H2O(g),一定条件下,现有两个体积均为1.0L恒容密闭容器甲和乙,在甲中充入0.1molCO2和0.2molH2,在乙中充入0.2molCO2和0.4molH2,发生上述反应并达到平衡.该反应中CO2的平衡转化率随温度的变化曲线如图所示.下列说法正确的是( )| A. | 反应2CO2(g)+6H2(g)$\stackrel{催化剂}{?}$CH3OCH3(g)+3H2O(g)的△S<0、△H<0 | |
| B. | 表示乙容器CO2的平衡转化率随温度变化的是曲线B | |
| C. | 体系中c(CH3OCH3):c(CH3OCH3,状态Ⅱ)<2c(CH3OCH3,状态Ⅲ) | |
| D. | 逆反应速率v逆:v逆(状态Ⅰ)<v逆(状态Ⅲ) |
15.设NA代表阿伏加德罗常数的数值,下列有关说法正确的是( )
| A. | 1mol乙烷含C-H键的数目为7NA | |
| B. | 1L0.5mol/LNa2S溶液中HS-的数目为0.5NA | |
| C. | 标准状况下,Na与水反应产生22.4 LH2时转移电子数目为2 NA | |
| D. | 含1mol HCOOH的水溶液中含氧原子的总数目为2NA |
 某温度时,在一个2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示.根据图中数据,回答下列问题:
某温度时,在一个2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示.根据图中数据,回答下列问题: