题目内容
可逆反应H2(g)+I2(s)2HI(g),在一定温度下,下列条件的变化中能使其平衡常数发生变化的是( )
| A、使I2(s)的表面积变大 |
| B、增大压强 |
| C、升高温度 |
| D、使用催化剂 |
考点:化学平衡常数的含义
专题:化学平衡专题
分析:化学平衡常数是温度的函数,正反应是吸热反应温度升高平衡常数变大,温度不变平衡常数不变.
解答:
解:化学平衡常数是温度的函数,正反应是吸热反应温度升高平衡常数变大,温度不变平衡常数不变,故选C.
点评:本题考查平衡常数的影响因素,温度是平衡常数的唯一影响因素,学生只要掌握这一点即可.

练习册系列答案
 华东师大版一课一练系列答案
华东师大版一课一练系列答案
相关题目
下列反应中既属于氧化还原反应,又属于吸热反应的是( )
A、C(石墨)=C(金刚石),在该反应进程中其能量变化如下图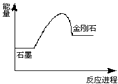 |
| B、Ba(OH)2?8H2O与NH4Cl反应 |
| C、灼热的碳与CO2反应 |
| D、甲烷在氧气中燃烧 |
下列四组物质,其中互为同分异构体的是( )
①苯和甲苯 ②1-丁炔和1,3-丁二烯 ③乙醇和乙二醇 ④乙烯和聚乙烯.
①苯和甲苯 ②1-丁炔和1,3-丁二烯 ③乙醇和乙二醇 ④乙烯和聚乙烯.
| A、①② | B、② | C、①③ | D、②③④ |
下列说法正确的是( )
| A、含有共价键的化合物一定是共价化合物 |
| B、不同元素原子形成的多原子分子中,含有的化学键只能是极性共价键 |
| C、非极性共价键只能存在于非金属单质或共价化合物中 |
| D、含有离子键的化合物一定是离子化合物 |
下列离子方程式中正确的是( )
| A、NaHSO4溶液和Ba(OH)2溶液充分反应后溶液呈中性:Ba2++2OH-+2H++SO4_2-=BaSO4↓+2H2O |
| B、向NH4Al(SO4)2溶液中滴入Ba(OH)2恰好使SO42-反应完全:2Ba2++4OH-+Al3++2SO42-═2BaSO4↓+AlO2-+2H2O |
| C、次氯酸钠溶液中通入SO2气体:2ClO-+SO2+H2O═2HClO+SO42- |
| D、Fe(OH)3溶于氢碘酸中:Fe(OH)3+3H+=Fe3++3H2O |
与第二周期稀有气体元素的原子具有相同电子数的微粒是( )
| A、S2-? |
| B、NH4+ |
| C、Cl-? |
| D、K+ |
设C+CO2?2CO;(正反应为吸热反应;反应速率为v1),2SO2+O2?2SO3;(正反应为放热反应;反应速率为v2),对于上述反应,当温度升高时,v1和v2的变化情况为( )
| A、v1 与v2同时增大 |
| B、v1 与v2同时减小 |
| C、v1增大,v2减小 |
| D、v1减小,v2增大 |
在恒温恒压密闭容器M(如图Ⅰ)和恒温恒容密闭容器N(如图Ⅱ)中,分别加入a molA和a molB,起始时两容器体积均为VL,发生如下反应并达到化学平衡状态:2A(?)+B(?)?xC(g)△H<0,平衡时M中A、B、C的物质的量之比为1:3:4.下列判断不正确的是( )


| A、x=2 |
| B、若N中气体的密度如图Ⅲ所示,则A、B只有一种是气态 |
| C、A为气体,B为非气体,则平衡时M、N中C的物质的量相等 |
| D、若A、B均为气体,平衡时M中A的转化率小于N中A的转化率 |
 将反应Cu+2FeCl3=CuCl2+2FeCl2设计成原电池,在图框中画出原电池的装置图,标出正、负极,并写出电极反应式.
将反应Cu+2FeCl3=CuCl2+2FeCl2设计成原电池,在图框中画出原电池的装置图,标出正、负极,并写出电极反应式.