题目内容
与第二周期稀有气体元素的原子具有相同电子数的微粒是( )
| A、S2-? |
| B、NH4+ |
| C、Cl-? |
| D、K+ |
考点:质子数、中子数、核外电子数及其相互联系
专题:原子组成与结构专题
分析:第二周期稀有气体元素为Ne,其原子具有电子数为10,阳离子的电子数=质子数-电荷数,阴离子的电子数=质子数+电荷数.
解答:
解:第二周期稀有气体元素为Ne,其原子具有电子数为10,阳离子的电子数=质子数-电荷数,阴离子的电子数=质子数+电荷数,
A、S2-电子数为16+2=18,故A不选;
B、NH4+的电子数为7+4×1-1=10,故B选;
C、Cl-的电子数为17+1=18,故C不选;
D、K+的电子数为19-1=18,故D不选;
故选B.
A、S2-电子数为16+2=18,故A不选;
B、NH4+的电子数为7+4×1-1=10,故B选;
C、Cl-的电子数为17+1=18,故C不选;
D、K+的电子数为19-1=18,故D不选;
故选B.
点评:本题考查了微粒核外电子数的计算,明确阳离子的电子数=质子数-电荷数,阴离子的电子数=质子数+电荷数是解决本题的关键,题目难度不大.

练习册系列答案
相关题目
下列方法中可以说明2HI(g)?H2(g)+I2(g)已达到平衡的是( )
| A、c(HI):c(H2):c(I2)=2:1:1时 |
| B、温度和体积一定时,混合气体的颜色不再改变 |
| C、单位时间内生成n mol H2的同时消耗2n mol HI |
| D、温度和体积一定时,容器内压强不再变化 |
可逆反应H2(g)+I2(s)2HI(g),在一定温度下,下列条件的变化中能使其平衡常数发生变化的是( )
| A、使I2(s)的表面积变大 |
| B、增大压强 |
| C、升高温度 |
| D、使用催化剂 |
下列各电离方程式中,书写正确的是( )
| A、H2S?2H++S2- |
| B、KHSO4?K++H++SO42- |
| C、Al(OH)3═Al3++3OH- |
| D、NaH2PO4═Na++H2PO4- |
有36g1H35Cl和80g3H37Cl,下列说法正确的是( )
| A、两者所含中子数之比为1:2 |
| B、分别与足量Na反应时,两者生成气体的质量之比为1:6 |
| C、与NaOH溶液发生中和反应所消耗的NaOH的物质的量之比为1:1 |
| D、两者所含质子数之比为9:22 |
根据原子序数,下列各组原子能以共价键结合的是( )
| A、12与9 | B、6与8 |
| C、11与17 | D、16与19 |
对A(g)+3B(g)=2C(g)+2D(g)来说,下列四种不同情况下的反应速率最快的是( )
| A、υ(A)=0.005mol/(L?s) |
| B、υ(B)=0.6mol/(L?min) |
| C、υ(C)=0.5mol/(L?min) |
| D、υ(D)=0.45mol/(L?min) |
某元素二价阳离子核外有10个电子,质量数为24,该元素原子的原子核中的中子数( )
| A、12 | B、14 | C、16 | D、18 |
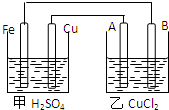 据图回答以下问题:
据图回答以下问题: