题目内容
9.下列离子反应不正确的是( )| A. | FeCl2溶液中通入Cl2:2 Fe2++Cl2=2 Fe3++2Cl- | |
| B. | Al2O3与NaOH溶液反应:Al2O3+2OH-=2 AlO2-+H2O | |
| C. | FeCl3溶液与铜:Fe3++Cu=Fe2++Cu2+ | |
| D. | Cl2溶于水:Cl2+H2O=2H++Cl-+ClO- |
分析 A.氯化亚铁与氯气反应生成氯化铁;
B.氧化铝与氢氧化钠溶液反应生成偏铝酸钠和水;
C.离子方程式两边正电荷不相等,违反了电荷守恒;
D.氯气与水反应生成氯化氢和次氯酸,次氯酸不能拆开.
解答 解:A.FeCl2溶液中通入Cl2,反应生成氯化铁,反应的离子方程式为:2Fe2++Cl2=2Fe3++2Cl-,故A正确;
B.Al2O3与NaOH溶液反应生成偏铝酸钠和水,反应的离子方程式为:Al2O3+2OH-=2 AlO2-+H2O,故B正确;
C.FeCl3溶液与铜反应生成氯化亚铁和氯化铜,正确的离子方程式为:2Fe3++Cu=2Fe2++Cu2+,故C错误;
D.氯气溶于水生成氯化氢和次氯酸,次氯酸小于保留分子式,正确的离子方程式为:Cl2+H2O=H++Cl-+HClO,故D错误;
故选CD.
点评 本题考查了离子方程式的判断,为高考的高频题,属于中等难度的试题,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等)等.

练习册系列答案
相关题目
19.已知某温度下CH3COOH和NH3•H2O的电离常数相等,现向10mL浓度为0.1mol•L-1的CH3COOH溶液中滴加相同浓度的氨水,在滴加过程中不正确的是( )
| A. | 反应前,两溶液由水电离的H+浓度相同 | |
| B. | 当加入氨水的体积为10mL时,c(NH4+)=c(CH3COO-) | |
| C. | 若醋酸溶液加水稀释,溶液中各离子浓度与c(CH3COO-)/c(H+)均减小 | |
| D. | 相同温度,相同浓度的CH3COONH4 与 NaCl溶液,对水的电离程度的影响前者大于后者 |
20.某化学教师为“氯气与金属钠反应”设计了如下装置与操作以替代相关的课本实验.
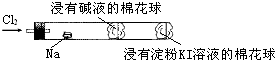
实验操作:先给钠预热,到钠熔融成圆球时,撤火,通入氯气,即可见钠着火燃烧,并产生大量白烟.以下叙述错误的是( )

实验操作:先给钠预热,到钠熔融成圆球时,撤火,通入氯气,即可见钠着火燃烧,并产生大量白烟.以下叙述错误的是( )
| A. | 钠着火燃烧产生苍白色火焰 | |
| B. | 反应生成的大量白烟是氯化钠晶体 | |
| C. | 管中部塞一团浸有NaOH溶液的棉球是用于吸收过量的氯气,以免其污染空气 | |
| D. | 管右端棉球外颜色变化可判断氯气是否被碱液完全吸收 |
17.有机物 的名称和一氯代物的种数是( )
的名称和一氯代物的种数是( )
 的名称和一氯代物的种数是( )
的名称和一氯代物的种数是( )| A. | 2,4,5-三甲基-4-乙基己烷,7种 | B. | 2,4-二甲基-4-异丙基己烷,8种 | ||
| C. | 2,4-二甲基-3-异丙基己烷,7种 | D. | 2,3,5-三甲基-3-乙基己烷,8种 |
4.下列离子方程式书写正确的是( )
| A. | 大理石和稀盐酸反应:2H++CO32-═CO2↑+H2O | |
| B. | 金属钠投入水中:2Na+2H2O═2Na++2OH-+H2↑ | |
| C. | 氧化铝和氢氧化钠溶液反应:Al2O3+OH-═AlO2-+H2O | |
| D. | 稀硝酸溶液中加入过量铁粉:Fe+4H++NO3-═Fe3++NO↑+2H2O |
1.化学与社会、生活密切相关,下列说法正确的是( )
| A. | “歼-20”飞机上使用的碳纤维是一种新型的有机高分子材料 | |
| B. | 用活性炭为糖浆脱色和用臭氧漂白纸浆,原理相似 | |
| C. | 燃料电池的燃料都在负极发生氧化反应 | |
| D. | Fe3O4俗称铁红,常做红色油漆和涂料 |