题目内容
下列实验操作或装置可以达到实验目的或符合实际的是( )
A、 称量一定量的NaOH固体 |
B、 量取9.3mL稀盐酸 |
C、 转移液体 |
D、 铜锌原电池实验 |
考点:化学实验方案的评价
专题:实验设计题
分析:A.称量氢氧化钠固体,应将氢氧化钠放在小烧杯中;
B.量取一定体积的液体,所用量筒应尽可能与溶液体积相近,以减小误差;
C.转移液体时,应防止液体外溅;
D.电子流向错误.
B.量取一定体积的液体,所用量筒应尽可能与溶液体积相近,以减小误差;
C.转移液体时,应防止液体外溅;
D.电子流向错误.
解答:
解:A.氢氧化钠易潮解,称量氢氧化钠固体,应将氢氧化钠放在小烧杯中,以减小称量误差,故A正确;
B.应用10mL量筒量取,以减小实验误差,故B错误;
C.转移液体时,玻璃棒不能紧贴容量瓶口,应防止液体外溅,故C错误;
D.锌为负极,铜为正极,电子由负极经导线流向正极,故D错误.
故选A.
B.应用10mL量筒量取,以减小实验误差,故B错误;
C.转移液体时,玻璃棒不能紧贴容量瓶口,应防止液体外溅,故C错误;
D.锌为负极,铜为正极,电子由负极经导线流向正极,故D错误.
故选A.
点评:本题考查较为综合,涉及药品的称量、溶液的配制、液体的量取以及原电池知识,为高考常见题型和高频考点,侧重于学生的分析能力和实验能力的考查,注意把握实验的原理和方法,难度不大.

练习册系列答案
相关题目
有关电化学知识的描述正确的是( )
| A、CaO+H2O═Ca(OH)2,可以放出大量的热,故可把该反应设计成原电池,把其中的化学能转化为电能 |
| B、某原电池反应为Cu+2AgNO3═Cu(NO3)2+2Ag,装置中的盐桥中可以是由KCl饱和溶液制得的琼脂 |
| C、因为铁的活动性强于铜,所以将铁、铜用导线连接后放入浓硝酸中,若能组成原电池,必是铁作负极,铜作正极 |
| D、理论上说,任何能自发进行的氧化还原反应都可被设计成原电池 |
实验是化学研究的基础,图中所示的实验方法、装置或操作完全正确的是( )
已知:氯气不溶于饱和食盐水.
已知:氯气不溶于饱和食盐水.
A、 除去混有的杂质气体 |
B、 浓硫酸稀释 |
C、 分离出AgNO3溶液中AgCl |
D、 称量30.46g的NaOH固体 |
化学用语是学习化学的重要工具.下列化学用语正确的是( )
| A、醋酸钠的水解:CH3COO-+H2O=CH3COOH+OH- |
| B、碳酸氢钠的水解:HCO3-+H2O?H3O++CO32- |
| C、硫酸氢钠溶液与氢氧化铝反应:H++OH-=H2O |
| D、碳酸氢钾与氢氧化钾溶液反应:HCO3-+OH-=H2O+CO32- |
设NA代表阿伏伽德罗常数,下列说法正确的是( )
| A、标准状况下,11.2L SO3含有0.5NA分子 |
| B、1mol Na2O2和足量的CO2反应转移的电子数为2NA |
| C、常温常压下,32g O2和O3混合气体所含氧原子数一定是2NA |
| D、22.4L CO和CO2的混合气体中所含的碳原子数一定是NA |
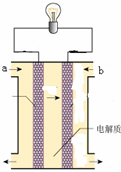 如图所示是一个燃料电池的示意图,当燃料电池如下时,其分析中正确的是( )
如图所示是一个燃料电池的示意图,当燃料电池如下时,其分析中正确的是( )| A、如果a极通入H2,b极通入O2,NaOH溶液作电解质溶液,则通H2的电极上发生的反应为:H2-2e-=2H+ |
| B、如果a极通入H2,b极通入O2,H2SO4溶液作电解质溶液,则通O2的电极上发生的反应为:O2+4e-+2H2O=4OH- |
| C、如果a极通入CH4,b极通入O2,NaOH作电解质溶液,则通CH4的电极上发生的反应为:CH4-8e-+10 OH-=CO32-+7H2O |
| D、如果a极通入H2,b极通入O2,NaOH溶液作电解质溶液,则溶液中的OH-离子向b极附近移动 |
下列说法正确的是( )
| A、SO3溶于水能导电,但SO3是非电解质 |
| B、酸、碱、盐是电解质,都有很强的导电能力 |
| C、电解质在水中一定能导电,在水中导电的化合物一定是电解质 |
| D、纯水的导电性很差,所以水不是电解质 |