题目内容
1.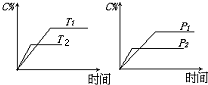 可逆反应mA(s)+nB(g)?eC(g)+fD(g),反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如图,下列叙述正确的是( )
可逆反应mA(s)+nB(g)?eC(g)+fD(g),反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如图,下列叙述正确的是( )| A. | 达平衡后,加入催化剂则C%增大 | |
| B. | 达平衡后,若升温,平衡向逆方向移动 | |
| C. | 化学方程式中n>e+f | |
| D. | 达平衡后,增加A的量有利于平衡向正方向移动 |
分析 图中有三个变量:C的百分含量、温度、时间,分析该图时应按照:先拐先平,高温高压的原则,则T2>T1,温度高C的百分含量反而低,说明升温平衡向逆反应方向移动;P2>P1,压强高C的百分含量反而低,说明升压平衡向逆反应方向移动,即b<c+d;以此分析解答.
解答 解:A.加入催化剂平衡不移动,故A错误;
B.从左图可知,T1<T2,T1→T2,温度升高,C的百分含量(C%)减小,平衡向逆向移动,故B正确;
C.从右图可知,P2>P1,P1→P2,压强增大,C的百分含量(C%)减小,平衡向逆向移动,根据加压平衡向气体体积缩小的方向移动得:n<e+f,故C错误;
D.A为固体,增加固体的量平衡不发生移动,故D错误;
故选B.
点评 本题考查了平衡移动的方向和读图能力,题目难度较小,读图时注意先拐先平,高温高压的原则.

 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案50mL 1.Omol·L—1盐酸跟50mL 1.1mol·L—1氢氧化钠溶液在图所示装置中进行中和反应,并通过测定反应过程中所放出的热量来计算中和热。试回答下列问题:

(1)大小烧杯间填满碎泡沫塑料的作用是_______________。
(2)_________(填“能”或“不能”)将环形玻璃搅拌棒改为环形金属(如铜)棒。其原因是__________________。
(3)大烧杯上如不盖硬纸板,对求得中和热数值的影响是________(填“偏高”“偏低”或“无影响”)。
(4)如果改用60mL 1.Omol·L—1盐酸跟50mL 1.1mol·L—1氢氧化钠溶液进行反应,则与上述实验相比,所放热量_______(填“增加” “减少”或“不变”),理由是_____________;所求中和热数值_________(填“增加”“减少”或“不变”),理由是_______________;
(5)________(填“能”或“不能”)用Ba(OH)2和硫酸代替盐酸和氢氧化钠溶液,理由是______________________.
(6)Q=cm△t,其中Q表示此中和反应放出的热量,m表示反应后混合液的质量,c表示反应后混合溶液的比热容,△t表示反应前后溶液的温度的差值。该实验小组做了三次实验,每次取溶液各50mL,并记录如下原始数据。
实验序号 | 起始温度t1/℃ | 终止温度/t2/℃ | 温差(t2-t1)/ ℃ |
1 | 25.0 | 32.6 | |
2 | 25.1 | 31.8 | |
3 | 25.1 | 31.9 |
已知盐酸、NaOH溶液密度近似为1.00g/cm3,中和后混合液的比热容c=4.184×10—3kJ/(g·℃),则该反应的中和热为△H=____________(保留小数点后一位)。
(7)上述实验数值结果与57.3kJ/mol有偏差,产生偏差的原因可能是_______(填字母)。
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰 视读数
视读数
C.分多次把NaOH溶液倒入盛有盐酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定HCl溶液的温度
| A. | 升温 | B. | 加压 | C. | 增加D的量 | D. | 加入催化剂 |
| A. | 水;无水CaCl2 固体 | B. | 饱和NaHCO3 溶液; 浓H2SO4 | ||
| C. | 浓H2SO4; 饱和NaHCO3 溶液 | D. | 饱和NaHCO3 溶液; 稀H2SO4 |
| A. | x+y<n | B. | 该化学平衡向正方向移动 | ||
| C. | B的转化率增大 | D. | C的体积分数减小 |
 现有A、B、D、E、F、G六种前四周期元素,它们的原子序数依次增大,E、F同主族,A、B的最外层电子数之和与D的最外层电子数相等,A、D、E的质子数之和与F的原子序数相等,A能分别与B、D、E形成电子总数相等的分子.E、F均能形成多种同素异形体,G2+的3d能级有8个电子.
现有A、B、D、E、F、G六种前四周期元素,它们的原子序数依次增大,E、F同主族,A、B的最外层电子数之和与D的最外层电子数相等,A、D、E的质子数之和与F的原子序数相等,A能分别与B、D、E形成电子总数相等的分子.E、F均能形成多种同素异形体,G2+的3d能级有8个电子. .(不考虑空间构型)
.(不考虑空间构型)