题目内容
9.已知:可逆反应A(g)+B(g)?2C(g)+D(s)△H<0,一定条件下达到平衡后,改变下列条件,一定能使平衡向逆反应方向移动的是( )| A. | 升温 | B. | 加压 | C. | 增加D的量 | D. | 加入催化剂 |
分析 可逆反应A(g)+B(g)?2C(g)+D(s)△H<0,反应是气体体积不变的放热反应,依据化学平衡移动原理分析影响化学平衡的因素,
A.该反应为放热反应,降温平衡正向进行,升温平衡逆向进行;
B.反应前后气体体积不变,改变压强,平衡不发生移动;
C.D为固体不影响化学平衡;
D.催化剂只能改变反应速率不改变化学平衡;
解答 解:A.改变温度一定改变化学平衡,反应为放热反应,降温一定能使平衡正向进行,升温一定能使平衡向逆反应方向移动,故A正确;
B.反应前后气体体积不变,增大压强,反应速率增大,化学平衡不发生移动,故B错误;
C.D为固体不影响化学平衡,增加D的量不影响化学平衡,平衡不动,故C错误;
D.催化剂只能改变反应速率不改变化学平衡,加入催化剂平衡不移动,故D错误;
故选A.
点评 本题考查了化学平衡的影响因素分析,注意固体不影响化学平衡,温度改变一定会改变化学平衡,掌握基础是关键,题目不难.

练习册系列答案
相关题目
4.二氧化碳和钠在一定条件下可制得金刚石,其化学方程式为3CO2+4Na═2X+C(金刚石).设NA为阿伏加德罗常数的值,下列有关此反应的叙述中,不正确的是( )
| A. | 1 mol C(金刚石)中含有C-C键的数目为2NA | |
| B. | 当有0.4 mol Na参与反应时,被还原的CO2为0.3NA | |
| C. | 金刚石与石墨之间的转化为化学变化 | |
| D. | X的化学式为Na2CO3 |
14.在一定温度固定容积的密闭容器中充入2molNO2发生反应2NO2(g)?N2O4(g)达到平衡后,在恒温恒容条件下,再向容器内通入2molNO2,又达到新平衡时NO2的体积分数( )
| A. | 不变 | B. | 增大 | C. | 减小 | D. | 无法判断 |
1.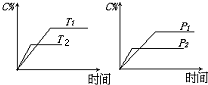 可逆反应mA(s)+nB(g)?eC(g)+fD(g),反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如图,下列叙述正确的是( )
可逆反应mA(s)+nB(g)?eC(g)+fD(g),反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如图,下列叙述正确的是( )
 可逆反应mA(s)+nB(g)?eC(g)+fD(g),反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如图,下列叙述正确的是( )
可逆反应mA(s)+nB(g)?eC(g)+fD(g),反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如图,下列叙述正确的是( )| A. | 达平衡后,加入催化剂则C%增大 | |
| B. | 达平衡后,若升温,平衡向逆方向移动 | |
| C. | 化学方程式中n>e+f | |
| D. | 达平衡后,增加A的量有利于平衡向正方向移动 |
16.下列物质的转化均能通过一步反应实现的是( )
| A. | NaAlO2→Al(OH)3→Al | B. | N2→NO2→HNO3 | ||
| C. | NaOH→Na2CO3→NaHCO3 | D. | FeS2→SO3→H2SO4 |
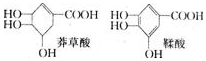
 反应是 ( )
反应是 ( )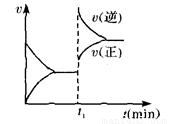
 4NO(g)+6H2O(g) △H<0
4NO(g)+6H2O(g) △H<0