题目内容
将一定质量的Mg、Zn、Al混合物与足量的稀H2SO4反应,生成H2 6.72L(标准状况),则原混合物的质量可能是( )
| A、2g | B、4g | C、8g | D、20g |
考点:化学方程式的有关计算,有关混合物反应的计算
专题:计算题
分析:三种金属中产生等量的氢气质量最大的为锌,质量最小的为铝.用极端假设法进行分析,假设混合物全部是锌或全部是铝,根据生成氢气,分别计算出它们的质量,混合物的质量介于最大值和最小值之间的值,据此判断.
解答:
解:标况下,6.72L氢气的物质的量为n=
=
=0.3mol,
设要生成H20.3mol需要锌的质量为y,则:
Zn+H2SO4═ZnSO4+H2↑
65g 1mol
y 0.3mol
解得y=
=19.5g
设要生成H2 0.3mol需要铝的质量为z,则:
2Al+3H2SO4═Al2(SO4)3+3H2↑
54g 3mol
z 0.3mol
解得z=
=5.4g
所以混合物的质量介于5.4g~19.5g
故选C.
| V |
| Vm |
| 6.72L |
| 22.4L/mol |
设要生成H20.3mol需要锌的质量为y,则:
Zn+H2SO4═ZnSO4+H2↑
65g 1mol
y 0.3mol
解得y=
| 65g×0.3mol |
| 1mol |
设要生成H2 0.3mol需要铝的质量为z,则:
2Al+3H2SO4═Al2(SO4)3+3H2↑
54g 3mol
z 0.3mol
解得z=
| 54g×0.3mol |
| 3mol |
所以混合物的质量介于5.4g~19.5g
故选C.
点评:本题考查混合物的有关计算,难度中等,解答本题关键是用极端假设法考虑问题的思路,“极端假设法”是用数学方法解决化学问题的常用方法,可分别假设原混合物是某一纯净物,计算出各自的质量,混合物的质量介于最大值和最小值之间.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
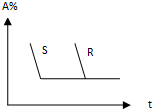 图中曲线R表示反应 A+B?C+D体系中A的百分含量与反应时间t的关系,曲线S是在R的基础上发生某种条件的改变造成的变化关系,对于R至S所改变的条件的说法中一定正确的是( )
图中曲线R表示反应 A+B?C+D体系中A的百分含量与反应时间t的关系,曲线S是在R的基础上发生某种条件的改变造成的变化关系,对于R至S所改变的条件的说法中一定正确的是( )| A、增高温度 |
| B、增大压强 |
| C、使用了正催化剂 |
| D、增大了A的浓度 |
下列叙述不正确的是( )
| A、在苯的同系物中,加入少量酸性高锰酸钾溶液,振荡后褪色的原因是侧链受苯环影响,易被氧化 |
B、 和 和 均为环状烃, 均为环状烃, 既是芳香烃又是芳香化合物 既是芳香烃又是芳香化合物 |
| C、已知二氯苯的同分异构体有三种,从而可以推知四氯苯的同分异构体数目也是3种 |
| D、分子式为C2H6O的红外光谱图上发现有C-H键和C-O键的振动吸收,由此推测可能有H-O键 |
下列说法正确的是( )
| A、NaOH固体溶于水后能导电,所以NaOH是电解质 |
| B、CO2的水溶液能够导电,所以CO2是电解质 |
| C、液态的铜导电性很好,所以铜是电解质 |
| D、盐酸能电离出H+和Cl-,所以盐酸属于电解质 |
下列说法正确的是( )
| A、碘盐中的碘可以直接用淀粉检验 |
| B、凡含有食品添加剂的食物对人体健康均有害,不可食用 |
| C、棉、麻、丝、毛及合成纤维完全燃烧都只生成CO2和H2O |
| D、维生素C具有还原性,可用作食品抗氧化剂 |
体积为VmL,密度为dg?cm-3的溶液,含有相对分子质量为M的溶质mg,其物质的量浓度为cmol?L-1,质量分数为w%,下列表达式正确的是( )
A、c=
| ||
B、m=V×d×
| ||
| C、w%=(c×M)(1 000×d)% | ||
D、c=
|
下列模型分别是HCN、S8、SF6、B12结构单元,下列说法错误的是( )

| A、32gS8分子中含有0.125molsp3-sp3σ键 |
| B、SF6是由极性键构成的正八面体分子 |
| C、1molHCN分子中有2molσ键和2molπ键 |
| D、B12中仅含非极性键 |
 (1)处于平衡状态的时间段是
(1)处于平衡状态的时间段是