题目内容
体积为VmL,密度为dg?cm-3的溶液,含有相对分子质量为M的溶质mg,其物质的量浓度为cmol?L-1,质量分数为w%,下列表达式正确的是( )
A、c=
| ||
B、m=V×d×
| ||
| C、w%=(c×M)(1 000×d)% | ||
D、c=
|
考点:物质的量浓度的相关计算,溶液中溶质的质量分数及相关计算
专题:物质的量浓度和溶解度专题
分析:A.根据物质的量浓度与溶质质量分数的关系c=
进行计算;
B.根据m=ρV计算出溶液质量,再根据m(溶质)=m(溶液)×ω计算出溶液中溶质的质量;
C.根据c=
计算出溶质质量分数进行计算;
D.根据物质的量浓度c=
计算出溶液的物质的量浓度.
| 1000ρω |
| M |
B.根据m=ρV计算出溶液质量,再根据m(溶质)=m(溶液)×ω计算出溶液中溶质的质量;
C.根据c=
| 1000ρω |
| M |
D.根据物质的量浓度c=
| n |
| V |
解答:
解:A.溶液的物质的量浓度为:c=
=
=
,故A错误;
B.溶液的质量为:dg?cm-3×VmL=dVg,溶液中溶质的质量为:dV×w%,故B正确;
C.根据c=
可得,溶质质量分数为:w%=
,故C错误;
D.溶液中溶质的物质的量为:n=
mol,溶液的体积为:0.001VL,则该溶液的浓度为:c=
=
,故D正确;
故选BD.
| 1000ρω |
| M |
| 1000×d×w% |
| M |
| 10dw |
| M |
B.溶液的质量为:dg?cm-3×VmL=dVg,溶液中溶质的质量为:dV×w%,故B正确;
C.根据c=
| 1000×d×w% |
| M |
| cM |
| 1000d |
D.溶液中溶质的物质的量为:n=
| m |
| M |
| ||
| 0.001VL |
| 1000m |
| MV |
故选BD.
点评:本题考查了物质的量浓度、溶质质量分数的计算,题目难度中等,注意掌握物质的量浓度、溶质质量分数的表达式及计算方法,试题培养了学生灵活应用所学知识的能力.

练习册系列答案
相关题目
下列实验现象的描述错误的是( )
| A、铜片投入到稀硫酸中产生大量的气泡 |
| B、打开盛有浓盐酸的试剂瓶盖时,瓶口出现白雾 |
| C、汞在空气中加热生成红色粉末 |
| D、硫在氧气中燃烧产生蓝紫色火焰 |
将一定质量的Mg、Zn、Al混合物与足量的稀H2SO4反应,生成H2 6.72L(标准状况),则原混合物的质量可能是( )
| A、2g | B、4g | C、8g | D、20g |
在密闭容器中发生如下反应:xA(g)+yB(g)?zC(g),达到平衡后测得A的浓度为0.20mol/L.在恒温下增大压强使容器容积缩小为原来的一半,再次达到平衡时,测得A的浓度为0.35mol/L.下列说法不正确的是( )
| A、x+y>z |
| B、平衡向右移动 |
| C、B的转化率提高 |
| D、C的体积分数降低 |
下列叙述不正确的是( )
| A、乙烯和植物油都能使酸性高锰酸钾褪色 |
| B、苯、乙酸都可与钠反应生成氢气 |
C、聚乙烯的结构简式为: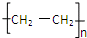 |
| D、灼烧闻气味可以区分棉织物和毛织物 |
在元素周期表中位于金属和非金属交界处容易找到的元素是( )
| A、制催化剂的元素 |
| B、制农药的元素 |
| C、半导体元素 |
| D、耐高温的合金元素 |
向Fe(OH)3胶体溶液中逐滴加入某种溶液,先有沉淀析出,继续加入该溶液时沉淀又溶解,则加入的溶液可能是( )
| A、0.5mol?L-1的硫酸镁溶液 |
| B、0.5 mol?L-1的氢氧化钠溶液 |
| C、0.5 mol?L-1的盐酸 |
| D、0.5 mol?L-1的氯化铵溶液 |