题目内容
下列有关化学基本概念的判断依据,正确的是( )
| A、溶液与胶体:本质区别是否均一、透明 |
| B、纯净物与混合物:是否仅含有一种物质 |
| C、氧化还原反应与非氧化还原反应:是否有单质参加 |
| D、强电解质与弱电解质:化合物溶液导电能力是否强 |
考点:分散系、胶体与溶液的概念及关系,混合物和纯净物,氧化还原反应,强电解质和弱电解质的概念
专题:物质的分类专题
分析:A、分散系的本质区别是分散质微粒直径大小;
B、依据含有物质种类物质分为混合物和纯净物;
C、有单质参加的反应不一定是氧化还原反应;
D、溶液的导电能力取决于离子浓度大小,与强弱电解质无直接关系;
B、依据含有物质种类物质分为混合物和纯净物;
C、有单质参加的反应不一定是氧化还原反应;
D、溶液的导电能力取决于离子浓度大小,与强弱电解质无直接关系;
解答:
解:A、分散系的本质区别是分散质微粒直径大小,溶液和胶体是均一稳定的分散系,胶体不一定透明,故A错误;
B、依据含有物质种类物质分为混合物和纯净物,含有一种物质的为纯净物,不同物质组成的物质为混合物,故B正确;
C、有单质参加的反应不一定是氧化还原反应,同素异形体的转化不是氧化还原反应,故C错误;
D、溶液的导电能力取决于离子浓度大小,与强弱电解质无直接关系,弱电解质溶液中离子浓度可以大于强电解质溶液中离子浓度,故D错误;
故选B.
B、依据含有物质种类物质分为混合物和纯净物,含有一种物质的为纯净物,不同物质组成的物质为混合物,故B正确;
C、有单质参加的反应不一定是氧化还原反应,同素异形体的转化不是氧化还原反应,故C错误;
D、溶液的导电能力取决于离子浓度大小,与强弱电解质无直接关系,弱电解质溶液中离子浓度可以大于强电解质溶液中离子浓度,故D错误;
故选B.
点评:本题考查了了分散系本质特征,强弱电解质的概念理解应用,掌握基础是关键,题目较简单.

练习册系列答案
相关题目
设NA表示阿伏加德罗常数的值,下列叙述中不正确的是( )
| A、常温常压下,1mol甲基(-CH3)含有的电子数为9NA |
| B、1 mol FeCl3跟水完全反应转化为氢氧化铁胶体后胶体粒子的数目小于NA |
| C、标况下,2.24LHF中含有的电子数为NA |
| D、1mol 金刚砂(SiC)中含有4NA碳硅键 |
0.2molNO和0.2molNO2相比较,下列说法不正确的是( )
| A、所占的体积一定相等 |
| B、所含分子数一定相等 |
| C、所含氮元素的质量一定相等 |
| D、所含原子总数之比为2:3 |
下列电子式中正确的是:( )
A、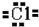 |
B、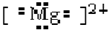 |
C、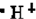 |
D、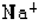 |
下列叙述中,正确的是( )
| A、金属氧化物都是碱性氧化物 |
| B、含金属元素的离子一定是阳离子 |
| C、金属阳离子被还原不一定得到金属单质 |
| D、某元素从化合态变为游离态时,该元素一定被还原 |
下列说法正确的是( )
| A、核磁共振氢谱图上可以推知有机物分子中几种不同类型的氢原子及它们的数目 |
| B、红外光谱是用高能电子流等轰击样品分子,使分子失去电子变成分子离子或碎片离子 |
| C、质谱法具有慢速、微量、精确的特点 |
| D、紫外光谱可以确定有机物中的化学键和官能团 |
2009年哥本哈根联合国气候变化大会的主题是约束温室气体的排放,遏制全球变暖.科学家们也积极探索利用CO2气体的新方法,例如人们已成功制得了CO2的原子晶体,利用CO2合成了可降解塑料聚二氧化碳等.下列说法正确的是( )
| A、二氧化碳是主要的大气污染物 |
| B、聚二氧化碳塑料可以通过加聚反应制得 |
| C、CO2原子晶体具有较低的熔点和沸点 |
| D、CO2的原子晶体和聚二氧化碳塑料都属于纯净物 |