题目内容
18.将19.2gCu和一定量浓HNO3反应,随着Cu的不断减少,反应生成气体的颜色逐渐变浅,当Cu反应完毕时,共收集到气体11.2L(标准状况),则反应中消耗HNO3的物质的量为1.1mol若将生成的气体与一定量O2混合后通入水中被完全吸收,需标准状况下O23.36L.分析 n(Cu)=$\frac{19.2g}{64g/mol}$=0.3mol,与硝酸反应生成Cu(NO3)2、NO和NO2,气体的物质的量为$\frac{11.2L}{22.4L/mol}$=0.5mol,结合N元素守恒、电子守恒计算;若将生成的气体与一定量O2混合后通入水中被完全吸收,最终氮变成+5价,实质相当铜给电子直接给氧气,根据得失电子守恒分析解答.
解答 解:n(Cu)=$\frac{19.2g}{64g/mol}$=0.3mol,气体的物质的量为$\frac{11.2L}{22.4L/mol}$=0.5mol,由N原子守恒可知,原子守恒得生成硝酸铜需要的n(HNO3)=2n[Cu(NO3)2]=2n(Cu)=2×0.3mol=0.6mol,气体为氮氧化物,气体的物质的量=n(NO)+n(NO2)=0.5mol,根据N元素守恒可知共消耗硝酸的物质的量为0.6mol+0.5mol=1.1mol,n(O2)
=$\frac{1}{2}$n(Cu)=0.3mol×$\frac{1}{2}$=0.15mol,所以需标准状况下O2的体积为:0.15mol×22.4L/mol=3.36L,故答案为:1.1mol;3.36.
点评 本题考查氧化还原反应的计算,为高频考点,把握电子守恒、原子守恒为解答的关键,侧重分析与计算能力的考查,题目难度不大.

练习册系列答案
 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案
相关题目
8.下列方程式书写正确的是( )
| A. | NaHSO4在水溶液中的电离方程式:NaHSO4═Na++HSO4- | |
| B. | H2SO3的电离方程式:H2SO3?2H++SO32- | |
| C. | CaCO3的电离方程式:CaCO3═Ca2++CO32- | |
| D. | CO32-的水解方程式:CO32-+2H2O?H2CO3+2OH- |
6.在含有Fe3+、Fe2+、Al3+、NH4+的稀溶液中加入足量Na2O2固体,充分作用后,再加入过量稀盐酸,完全反应,则离子数目没有变化的是( )
| A. | Fe3+、Al3+ | B. | Fe3+ | C. | Fe2+、NH4+ | D. | Al3+ |
13.化学中常用类比的方法可预测许多物质的性质.如根据H2+Cl2═2HCl推测:H2+Br2═2HBr.但类比是相对的,如根据2Na2O2+2CO2═2Na2CO3+O2,推测2Na2O2+2SO2═2Na2SO3+O2是错误的,应该是Na2O2+SO2═Na2SO4.
下列各组类比中正确的是( )
下列各组类比中正确的是( )
| A. | 钠与水反应生成NaOH和H2,推测:所有金属与水反应都生成碱和H2 | |
| B. | 由CO2+Ca(ClO)2+H2O═CaCO3↓+2HClO,推测:2SO2+Ca(ClO)2+H2O═CaSO3↓+2HClO | |
| C. | 铝和硫直接化合能得到Al2S3,推测:铁和硫直接化合也能得到 Fe2S3 | |
| D. | 由Na2CO3+2HCl═2NaCl+H2O+CO2↑,推测:Na2SO3+2HCl═2NaCl+H2O+SO2↑ |
3.关于有机物 的下列叙述中,正确的是( )
的下列叙述中,正确的是( )
 的下列叙述中,正确的是( )
的下列叙述中,正确的是( )| A. | 它的系统名称是2,4-二甲基-4-戊烯 | |
| B. | 它的分子中最多有5个碳原子在同一平面上 | |
| C. | 它与甲基环己烷互为同分异构体 | |
| D. | 有机物的一氯取代产物共有4种 |
5.下列说法正确的是( )
| A. | 活化分子间所发生的碰撞都为有效碰撞 | |
| B. | 合成氨工业中用铁触媒做催化剂能用勒夏特列原理解释 | |
| C. | 升高温度能使化学反应速率增大的主要原因是增加了单位体积内活化分子的百分数 | |
| D. | 将钢闸门与电源的正极相连,是采用了外加电流的阴极保护法 |
6.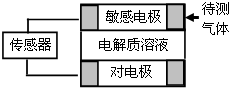 气体的自动化检测中常常应用原电池原理的传感器.如图为电池的工作示意图.气体扩散进入传感器,在敏感电极上发生反应,传感器就会接收到电信号.下表列出了待测气体及敏感电极上部分反应产物.则下列说法中正确的是( )
气体的自动化检测中常常应用原电池原理的传感器.如图为电池的工作示意图.气体扩散进入传感器,在敏感电极上发生反应,传感器就会接收到电信号.下表列出了待测气体及敏感电极上部分反应产物.则下列说法中正确的是( )
 气体的自动化检测中常常应用原电池原理的传感器.如图为电池的工作示意图.气体扩散进入传感器,在敏感电极上发生反应,传感器就会接收到电信号.下表列出了待测气体及敏感电极上部分反应产物.则下列说法中正确的是( )
气体的自动化检测中常常应用原电池原理的传感器.如图为电池的工作示意图.气体扩散进入传感器,在敏感电极上发生反应,传感器就会接收到电信号.下表列出了待测气体及敏感电极上部分反应产物.则下列说法中正确的是( )| 待测气体 | 部分电极产物 |
| NO2 | NO |
| Cl2 | HCl |
| CO | CO2 |
| SO2 | H2SO4 |
| A. | 上述气体检测时,敏感电极均作电池负极 | |
| B. | 检测分别含SO2和CO体积分数相同的两份体积相同的空气样本时,传感器上产生的电流大小相同 | |
| C. | 检测CO时,敏感电极上的电极反应式为CO+2OH--2e-═CO2+H2O | |
| D. | 检测NO2时,电解质溶液可选NaOH溶液 |