题目内容
14.归纳整理是科学学习的重要方法之一.在学习了元素周期表之后,有关氧族元素的各种性质,可归纳整理出如下表所示的表格(部分).| 性质\元素 | 8O | 16S | 34Se | 52Te |
| 单质熔点(℃) | -218.4 | 113 | 450 | |
| 单质沸点(℃) | -183 | 444.6 | 685 | 1390 |
| 主要化合价 | -2 | -2,+4,+6 | -2,+4,+6 | |
| 原子半径 | 逐渐增大 | |||
| 单质与H2反应 | 点燃时易化合 | 加热化合 | 加热难化合 | 不能直接化合 |
(1)硒的熔点范围可能是113℃~450℃
(2)碲的化合价可能有-2,+4,+6
(3)氢硒酸有较强的还原性(填“氧化性”或“还原性”),因此把它放在空气中长期保存容易变质,其可能发生的化学方程式为2H2Se+O2=2H2O+2Se↓.
分析 (1)由表可知:从氧到碲,单质的熔点逐渐升高;
(2)根据硒的化合价来推测;
(3)根据氢硒酸中硒的化合价为-2价,处于最低价,具有还原性,反应方程式为:2H2Se+O2=2H2O+2Se↓.
解答 解:(1)由表可知:从氧到碲,单质的熔点逐渐升高,所以硒的熔点范围可能是113℃~450℃,故答案为:113℃~450℃;
(2)因硒的化合价有-2,+4,+6,碲的性质与硒相似,所以碲的化合价可能有-2,+4,+6,故答案为:-2,+4,+6;
(3)因氢硒酸中硒的化合价为-2价,处于最低价,具有还原性,能被空气中的氧气氧化,反应方程式为:2H2Se+O2=2H2O+2Se↓,故答案为:还原性;2H2Se+O2=2H2O+2Se↓.
点评 本题主要考查了氧族元素的性质,考查了类推法的应用,应根据不同知识的特点类推,不能盲目类推,并注意知识点与方法的有机结合,做到具体问题能具体分析.

练习册系列答案
相关题目
4.常温下可以盛放浓硫酸的容器是( )
| A. | 塑料 | B. | Fe | C. | Al | D. | Mg |
5.下列说法中,不正确的是( )
| A. | 氯气可用于消毒和制造漂白粉 | B. | 氨气可用于制造氮肥 | ||
| C. | 乙烯可用于制造塑料 | D. | 铝制容器可用于盛放稀硫酸 |
2.铜锌合金的颜色酷似金的颜色,所以近来用铜锌合金制成的假金元宝欺骗行人的事件屡有发生.要检验市面上的金首饰是否为纯金或者真金,可取样品与一种试剂进行反应,根据现象即可判断,所取的试剂不能是( )
| A. | 硫酸 | B. | “王水” | C. | 盐酸 | D. | 硝酸 |
19.水溶液中能大量共存的一组离子是( )
| A. | K+、NH4+、OH-、SO42- | B. | H+、Fe2+、SO42-、ClO- | ||
| C. | Na+、Ca2+、Cl-、CO32- | D. | K+、Ca2+、Cl-、NO3- |
6.已知:1mol H2(g)与1mol Br2(g)完全反应生成2mol HBr(g)时放出72kJ的热量,有关物质的相关数据如下表:
则表中a为( )
| 化学键 | H2(g) | Br2(g) | HBr(g) |
| 断裂1mol化学键需要吸收的能量/kJ | 436 | a | 369 |
| A. | 404 | B. | 260 | C. | 230 | D. | 200 |
4.下列有关除杂质(括号中为杂质)的操作中,错误的是( )
| A. | 乙醇(水):加入足量生石灰充分振荡,蒸馏,收集馏出物 | |
| B. | CCl4(乙醇):多次加水,振荡,分液,弃水层 | |
| C. | 苯(己烯):加溴水,振荡,过滤除去沉淀 | |
| D. | 乙酸乙酯(乙酸):加饱和碳酸钠溶液,充分振荡,分液,弃水层 |


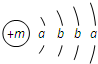 某种融雪剂,其主要成分的化学式为XY2,图为X原子的结构示意图,X的阳离子与Y的阴离子的电子层结构相同.元素Z、W均为短周期元素,它们原子的最外层电子数均是其电子层数的2倍,Z与Y相邻且Z、W能形成一种WZ2型分子.
某种融雪剂,其主要成分的化学式为XY2,图为X原子的结构示意图,X的阳离子与Y的阴离子的电子层结构相同.元素Z、W均为短周期元素,它们原子的最外层电子数均是其电子层数的2倍,Z与Y相邻且Z、W能形成一种WZ2型分子.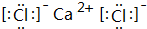 .
.