题目内容
4.下列有关除杂质(括号中为杂质)的操作中,错误的是( )| A. | 乙醇(水):加入足量生石灰充分振荡,蒸馏,收集馏出物 | |
| B. | CCl4(乙醇):多次加水,振荡,分液,弃水层 | |
| C. | 苯(己烯):加溴水,振荡,过滤除去沉淀 | |
| D. | 乙酸乙酯(乙酸):加饱和碳酸钠溶液,充分振荡,分液,弃水层 |
分析 根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答 解:A.乙醇(水):加入足量生石灰,氧化钙与水反应生成氢氧化钙;乙醇易挥发,蒸馏,收集馏出物,可用蒸馏分离,故A正确;
B.CCl4不溶于水,乙醇易溶于水,多次加水振荡,分液,弃水层可分开,故B正确;
C.苯能萃取溴水中的溴单质,己烯能和溴水加成,产物能和溴的苯溶液互溶,无法分离,故C错误;
D.乙酸的酸性强于碳酸,乙酸与碳酸钠反应2CH3COOH+Na2CO3=2CH3COONa+CO2↑+H2O,乙酸与碳酸钠反应后,与乙酸乙酯分层,则充分振荡,分液,弃水层得到乙酸乙酯,故D正确;
故选C.
点评 本题考查物质的分离和提纯试剂的选择以及操作,注意除杂是不能引入新的杂质、不能影响被提纯的物质的性质和量,并且操作简单可行,除杂时要结合物质的物理性质和化学性质进行分离,题目难度不大.

练习册系列答案
相关题目
14.归纳整理是科学学习的重要方法之一.在学习了元素周期表之后,有关氧族元素的各种性质,可归纳整理出如下表所示的表格(部分).
请根据上表回答下列问题:
(1)硒的熔点范围可能是113℃~450℃
(2)碲的化合价可能有-2,+4,+6
(3)氢硒酸有较强的还原性(填“氧化性”或“还原性”),因此把它放在空气中长期保存容易变质,其可能发生的化学方程式为2H2Se+O2=2H2O+2Se↓.
| 性质\元素 | 8O | 16S | 34Se | 52Te |
| 单质熔点(℃) | -218.4 | 113 | 450 | |
| 单质沸点(℃) | -183 | 444.6 | 685 | 1390 |
| 主要化合价 | -2 | -2,+4,+6 | -2,+4,+6 | |
| 原子半径 | 逐渐增大 | |||
| 单质与H2反应 | 点燃时易化合 | 加热化合 | 加热难化合 | 不能直接化合 |
(1)硒的熔点范围可能是113℃~450℃
(2)碲的化合价可能有-2,+4,+6
(3)氢硒酸有较强的还原性(填“氧化性”或“还原性”),因此把它放在空气中长期保存容易变质,其可能发生的化学方程式为2H2Se+O2=2H2O+2Se↓.
15.一定质量的甲烷燃烧后得到的产物为CO、CO2和水蒸气,此混合气体质量为67.2g,当其缓慢经过无水CaCl2时,CaCl2增重32.4g,则原混合气体中CO2的质量为( )
| A. | 8.4 g | B. | 26.4 g | C. | 30.2 g | D. | 34.8 g |
9.下列各分子中,化学键类型不同的是( )
| A. | H2O、CO | B. | MgF2、H2O | C. | KOH、Mg(OH)2 | D. | HCl、HBr |
16.下列各装置能构成原电池的是( )
| A. | 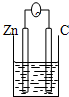 稀硫酸 | B. | 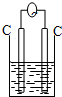 AgNO3(aq) | C. | 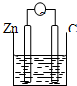 蔗糖 | D. | 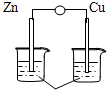 稀硫酸 |
13.根据下列实验操作和现象所得出的结论正确的是( )
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 将某溶液与稀盐酸反应产生的气体通入澄清石灰水 | 石灰水变浑浊 | 该溶液中一定含有CO32- |
| B | 常温下,将铁片浸入足量浓硫酸中 | 铁片不溶解 | 常温下,铁与浓硫酸一定没有发生化学反应 |
| C | 向某食盐溶液中滴加淀粉溶液 | 溶液颜色不变 | 该实验中一定没有添加KIO3 |
| D | 向苯酚钠溶液滴加乙酸溶液 | 溶液变浑浊 | 相同条件下,乙酸的酸性一定比苯酚强 |
| A. | A | B. | B | C. | C | D. | D |
14.有关能量的判断或表示方法正确的是( )
| A. | 由H+(aq)+OH-(aq)═H2O△H=-57.3 kJ/mol可知:含0.5 mol H2SO4的浓溶液与含1 mol NaOH的溶液混合,放出热量等于57.3 kJ | |
| B. | 从C(石墨)═C(金刚石)△H=+1.19 kJ/mol可知:金刚石比石墨更稳定 | |
| C. | 等质量的硫蒸气和硫固体分别完全燃烧,前者放出热量更多 | |
| D. | 2 g H2完全燃烧生成液态水放出285.8 kJ热量,则氢气燃烧的热化学方程式为2H2(g)+O2(g)═2H2O(l)△H=-285.8 kJ/mol-1 |