题目内容
16.欲将氯化钠、沙子(主要成分为SiO2)、碘三种物质组成的混合物分离,最合理的操作顺序是( )| A. | 溶解、过滤、加热(升华)、蒸发(结晶) | B. | 加热(升华)、溶解、过滤、蒸发(结晶) | ||
| C. | 升华、溶解、蒸馏、结晶 | D. | 溶解、结晶、过滤、升华 |
分析 碘易升华,先分离出碘,再利用SiO2不溶于水,先过滤分离出SiO2,滤液蒸发得到NaCl,以此来解答.
解答 解:将氯化钠、沙子(主要成分为SiO2)、碘三种物质组成的混合物分离,先加热(升华)分离出碘,溶解后过滤分离出沙子,最后对滤液蒸发(结晶)分离出氯化钠,即合理的操作顺序为加热(升华)、溶解、过滤、蒸发(结晶),
故选B.
点评 本题考查混合物分离提纯,为高频考点,把握物质的性质、性质差异及混合物分离方法等为解答的关键,侧重分析与应用能力的考查,注意碘易升华的特性,题目难度不大.

练习册系列答案
 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案
相关题目
2.下列有关自然界中氮循环(如图)的说法不正确的是( )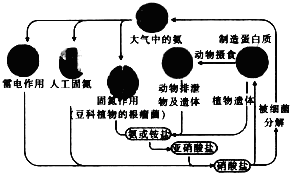

| A. | 含氮无机物和含氮有机物可相互转化 | |
| B. | 通过闪电产生NO属于高能固氮 | |
| C. | 硝酸盐被细菌分解为氮气过程氮元素一定被氧化 | |
| D. | C、H、O也参与自然界中氮循环 |
7.我国科学家屠呦呦因发明抗疟新药青蒿素(分子式:C15H22O5)荣获2015年诺贝尔医学奖.青蒿素属于( )
| A. | 混合物 | B. | 有机物 | C. | 氧化物 | D. | 单质 |
4.用NA表示阿伏加德罗常数的值.下列说法正确的是( )
| A. | 16g O3含有的氧原子数为NA | |
| B. | 常温常压下,22.4L SO2含有的分子数为NA | |
| C. | 1molMg变成Mg2+时,失去电子的数目为NA | |
| D. | 1L 1mol•L-1H2SO4溶液中含H+的数目为NA |
1.有a、b、c、d、e、f五种气体,进行下列实验:
a、b、c、d、e、f依次可能是( )
| 步 骤 | 现象 |
| (1)其中e气体是有色的,其余气体均为无色,a、f是两种常见的大气污染物 | |
| (2)a和b在常温下混合 | 气体变红棕色 |
| (3)c和d混合 | 能产生白烟 |
| (4)b、e、f分别通入氢硫酸中 | 都产生淡黄色浑浊 |
| A. | NO、O2、NH3、HCl、Cl2、SO2 | B. | NO、O2、NH3、HCl、SO2、Cl2 | ||
| C. | NO、O2、NH3、CO2、NO2、SO2 | D. | O2、NH3、NO、HCl、Cl2、SO2 |
5.工业上可用硫酸铝与硫黄焙烧制备氧化铝,再电解氧化铝制得铝,发生反应如下:
反应Ⅰ:2Al2(SO4)3+3S$\frac{\underline{\;高温\;}}{\;}$2Al2O3+9SO2↑,反应Ⅱ:2Al2O3$\frac{\underline{\;通电\;}}{\;}$4Al+3O2↑
下列说法中正确的是( )
反应Ⅰ:2Al2(SO4)3+3S$\frac{\underline{\;高温\;}}{\;}$2Al2O3+9SO2↑,反应Ⅱ:2Al2O3$\frac{\underline{\;通电\;}}{\;}$4Al+3O2↑
下列说法中正确的是( )
| A. | 反应Ⅰ中S单质是氧化剂 | |
| B. | 反应ⅡAl2O3中Al元素被氧化 | |
| C. | 当生成5.4 g Al时,反应Ⅰ和反应Ⅱ共转移1.2 mol e- | |
| D. | 反应Ⅰ氧化产物与还原产物物质的量之比为2:9 |
6.下列物质不能通过化合反应制得的是( )
| A. | SO3 | B. | Na2O2 | C. | Al(OH)3 | D. | NO |
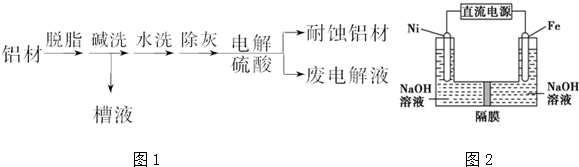
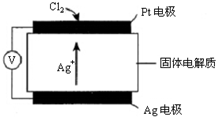 氯碱工业以电解精制饱和食盐水的方法制取氯气、氢气、烧碱,以及生产ClO2和氯的含氧酸盐(NaClO、NaClO3)等系列化工产品.
氯碱工业以电解精制饱和食盐水的方法制取氯气、氢气、烧碱,以及生产ClO2和氯的含氧酸盐(NaClO、NaClO3)等系列化工产品.