题目内容
17.运用元素周期律分析下面的推断,其中不正确的是( )| A. | 在氧气中,铷(Rb)的燃烧产物比钠的燃烧产物更复杂 | |
| B. | 砹(At)为有色固体,AgAt难溶于水也不溶于稀硝酸 | |
| C. | 由水溶液的酸性:HCl>H2S,可推断出元素的非金属性:Cl>S | |
| D. | 硅、锗都位于金属与非金属的交界处,都可以做半导体材料 |
分析 A.Li燃烧生成Li2O,Na燃烧生成Na2O2,碱金属的性质越活泼,燃烧产物越复杂;
B.卤素单质从上到下颜色加深、状态由气体、液体、固体变化,AgX不溶于水和酸(AgF除外);
C.不能利用氢化物的酸性比较非金属性;
D.位于金属与非金属的交界处的元素,具有金属性和非金属性.
解答 解:A.Li燃烧生成Li2O,Na燃烧生成Na2O2,碱金属的性质越活泼,燃烧产物越复杂,则铷(Rb)的燃烧产物比钠的燃烧产物更复杂,可能有超氧化物,故A正确;
B.卤素单质从上到下颜色加深、状态由气体、液体、固体变化,AgX不溶于水和酸(AgF除外),则砹(At)为有色固体,AgAt难溶于水也不溶于稀硝酸,故B正确;
C.不能利用氢化物的酸性比较非金属性,比较角度不合理,应利用氢化物的稳定性比较非金属性,故C错误;
D.位于金属与非金属的交界处的元素,具有金属性和非金属性,则硅、锗都位于金属与非金属的交界处,都可以做半导体材料,故D正确;
故选C.
点评 本题考查元素周期表和周期律,为高频考点,把握元素的位置、性质、元素周期律为解答的关键,侧重分析与应用能力的考查,注意规律性知识的应用,选项C为易错点,题目难度不大.

练习册系列答案
 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案 全程金卷系列答案
全程金卷系列答案
相关题目
7.软锰矿的主要成分为MnO2,含少量Al2O3和SiO2.闪锌矿主要成分为ZnS,含少量FeS、CuS、CdS杂质.现以软锰矿和闪锌矿为原料制备MnO2和Zn,其简化流程如图(中间产物的固体部分已经略去).

已知:
Ⅰ.矿石中所有金属元素在滤液A中均以离子形式存在.
Ⅱ.各种金属离子完全沉淀的pH如表:
回答下列问题:
(1)步骤①中为了加快硫酸的浸取速率,可采用的方法是将矿石粉碎、加热、搅拌等(任写一种).①中发生多个反应,其中MnO2、FeS与硫酸共热时有淡黄色物质析出,溶液变为棕黄色,写出MnO2、FeS与硫酸共热发生反应的化学方程式3MnO2+2FeS+6H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$3MnSO4+Fe2(SO4)3+2S+6H2O.
(2)步骤②加入金属锌是为了回收金属,回收金属的主要成分是Cu、Cd.
(3)步骤③中MnO2的其作用是将Fe2+氧化为Fe3+,另外一种物质X可以是AC.
A.ZnO B.MgCO3 C.MnCO3 D.Cu(OH)2
(4)MnO2与Li构成LiMnO2,它可作为某锂离子电池的正极材料,电池反应方程式为:Li1-xMnO2+LixC6=LiMnO2+6C,写出该锂离子电池的正极电极反应式Li1-xMnO2+xLi++xe-=LiMnO2.
(5)已知:HCN的电离常数K=4.9×10-10,H2S的电离常数K1=1.3×10-7,K2=7.0×10-15,向NaCN溶液中通入少量的H2S气体,反应的离子方程式为CN-+H2S=HCN+HS-.在废水处理领域中常用H2S将Mn2+转化为MnS除去,向含有0.020mol•L-1Mn2+废水中通入一定量的H2S气体,调节溶液的pH=a,当HS-浓度为1.0×10-4 mol•L-1时,Mn2+开始沉淀,则a=5.[已知:Ksp(MnS)=1.4×10-15].

已知:
Ⅰ.矿石中所有金属元素在滤液A中均以离子形式存在.
Ⅱ.各种金属离子完全沉淀的pH如表:
| Zn2+ | Mn2+ | Fe2+ | Fe3+ | Al3+ | |
| pH | 8.0 | 10.1 | 9.0 | 3.2 | 4.7 |
(1)步骤①中为了加快硫酸的浸取速率,可采用的方法是将矿石粉碎、加热、搅拌等(任写一种).①中发生多个反应,其中MnO2、FeS与硫酸共热时有淡黄色物质析出,溶液变为棕黄色,写出MnO2、FeS与硫酸共热发生反应的化学方程式3MnO2+2FeS+6H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$3MnSO4+Fe2(SO4)3+2S+6H2O.
(2)步骤②加入金属锌是为了回收金属,回收金属的主要成分是Cu、Cd.
(3)步骤③中MnO2的其作用是将Fe2+氧化为Fe3+,另外一种物质X可以是AC.
A.ZnO B.MgCO3 C.MnCO3 D.Cu(OH)2
(4)MnO2与Li构成LiMnO2,它可作为某锂离子电池的正极材料,电池反应方程式为:Li1-xMnO2+LixC6=LiMnO2+6C,写出该锂离子电池的正极电极反应式Li1-xMnO2+xLi++xe-=LiMnO2.
(5)已知:HCN的电离常数K=4.9×10-10,H2S的电离常数K1=1.3×10-7,K2=7.0×10-15,向NaCN溶液中通入少量的H2S气体,反应的离子方程式为CN-+H2S=HCN+HS-.在废水处理领域中常用H2S将Mn2+转化为MnS除去,向含有0.020mol•L-1Mn2+废水中通入一定量的H2S气体,调节溶液的pH=a,当HS-浓度为1.0×10-4 mol•L-1时,Mn2+开始沉淀,则a=5.[已知:Ksp(MnS)=1.4×10-15].
8.某气体的摩尔质量为M,分子质量为m.若1摩尔该气体的体积为Vm,密度为ρ,则该气体单位体积分子数为(阿伏伽德罗常数为NA)( )
| A. | $\frac{{N}_{A}}{{V}_{m}}$ | B. | $\frac{M}{m{V}_{m}}$ | C. | $\frac{ρ{N}_{A}}{M}$ | D. | $\frac{ρ{N}_{A}}{m}$ |
2.如图甲是一种利用微生物将废水中的尿素(H2NCONH2,氮元素显-3价)的化学能直接转化为电能,并生成对环境无害物质的装置,同时利用此装置的电能在铁上镀铜,下列说法中正确的是( )

| A. | H+透过质子交换膜由右向左移动 | |
| B. | 铜电极应与X相连接 | |
| C. | M电极的反应式:H2NCONH2+H2O-6e-═CO2↑+N2↑+6H+ | |
| D. | 当N电极消耗0.5 mol气体时,则铁电极增重32 g |
9.埋在地下的钢管道可以用如图所示方法进行电化学保护.下列说法正确的是( )

| A. | 该方法将电能转化成化学能 | |
| B. | 在此装置中钢管道作正极 | |
| C. | 该方法称为“外加电流的阴极保护法” | |
| D. | 镁块上发生的电极反应为O2+2H2O+4e-═4OH- |


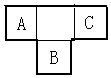 A、B、C为短周期元素,在周期表中所处的位置如图所示,A、C两元素的原子核外电子数之和等于B原子的质子数,B原子核内质子数和中子数相等.且含B元素物质的大量燃烧是形成酸雨的主要原因之一.
A、B、C为短周期元素,在周期表中所处的位置如图所示,A、C两元素的原子核外电子数之和等于B原子的质子数,B原子核内质子数和中子数相等.且含B元素物质的大量燃烧是形成酸雨的主要原因之一.  ,用电子式表示元素B的钠盐的形成过程:
,用电子式表示元素B的钠盐的形成过程: .
.