题目内容
下列叙述中正确的是( )
| A、在蔗糖中加入浓硫酸后出现发黑现象,说明浓硫酸具有脱水性 |
| B、向碘水中通入SO2,碘水褪色说明SO2具有漂白性 |
| C、蘸有浓硫酸的玻璃棒接近浓氨水瓶口有白烟产生 |
| D、某溶液加入BaCl2溶液,产生不溶于稀硝酸的白色沉淀,该溶液一定含有SO42- |
考点:浓硫酸的性质,二氧化硫的化学性质
专题:氧族元素
分析:A.浓硫酸能将蔗糖中H、O以水的形式脱去而体现脱水性;
B.二氧化硫和碘能发生氧化还原反应生成硫酸;
C.浓硫酸没有挥发性;
D.能和氯化钡反应生成不溶于稀硝酸的白色沉淀不仅硫酸根离子.
B.二氧化硫和碘能发生氧化还原反应生成硫酸;
C.浓硫酸没有挥发性;
D.能和氯化钡反应生成不溶于稀硝酸的白色沉淀不仅硫酸根离子.
解答:
解:A.浓硫酸能将蔗糖中H、O以2:1水的形式脱去,浓硫酸体现脱水性,故A正确;
B.二氧化硫和碘能发生氧化还原反应生成硫酸,SO2+I2+2H2O=2HI+H2SO4,该反应中二氧化硫体现还原性而不是漂白性,故B错误;
C.浓硫酸没有挥发性,所以蘸有浓硫酸的玻璃棒接近浓氨水瓶口没有白烟产生,故C错误
D.能和氯化钡反应生成不溶于稀硝酸的白色沉淀不仅硫酸根离子,还有银离子,故D错误;
故选A.
B.二氧化硫和碘能发生氧化还原反应生成硫酸,SO2+I2+2H2O=2HI+H2SO4,该反应中二氧化硫体现还原性而不是漂白性,故B错误;
C.浓硫酸没有挥发性,所以蘸有浓硫酸的玻璃棒接近浓氨水瓶口没有白烟产生,故C错误
D.能和氯化钡反应生成不溶于稀硝酸的白色沉淀不仅硫酸根离子,还有银离子,故D错误;
故选A.
点评:本题考查了物质的性质,根据浓硫酸的性质、离子的检验、二氧化硫的性质分析解答,注意B中二氧化硫的作用,知道硫酸根离子的检验试剂是盐酸酸化的氯化钡溶液,题目难度不大.

练习册系列答案
 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案
相关题目
下列叙述中,正确的是( )
| A、糖类化合物都具有相同的官能团 |
| B、乙醇和汽油都是可再生能源,所以要大力发展“乙醇汽油” |
| C、蛋白质的水解产物都含有羧基和羟基 |
| D、油脂的种类很多,但它们水解后都一定有一产物相同 |
对于常温下pH=3的醋酸溶液,下列说法正确的是( )
| A、C(H+)=c(CH3COO-)+c(OH-) | ||
B、室温下向10mL pH=3的醋酸溶液中加入水稀释,溶液中
| ||
| C、加入少量醋酸钠固体,溶液pH降低 | ||
| D、与等体积pH为11的NaOH溶液混合后所得溶液中:c(Na+)=c(CH3COO-) |
用如图装置进行实验(A为电流计),观察到现象:装置图1:Cu电极上产生大量的无色气泡;装置图2:Cu电极上无气泡产生,而Cr电极上产生大量气泡,则下列说法正确的是( )
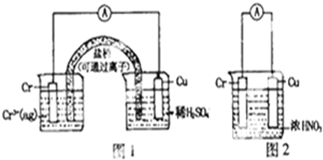

| A、图1是电解池,图2是原电池 |
| B、两个电池中,电子均由Cr电极流向Cu电极 |
| C、图2中Cr电极可能被浓HNO3钝化成惰性电极 |
| D、由实验现象可知金属活动性:Cu>Cr |
按照有机物的命名规则,下列命名正确的是( )
| A、CH2Br-CH2Br 二溴乙烷 |
| B、CH3OOCCH3 甲酸乙酯 |
C、 硬脂酸甘油脂 硬脂酸甘油脂 |
D、 3,3-二甲基-2-丁醇 3,3-二甲基-2-丁醇 |
下列说法正确的是( )
| A、1mol N2的质量是14g |
| B、H2SO4的摩尔质量是98g |
| C、H2O的摩尔质量是18g/mol |
| D、1mol HCl的质量是36.5g/mol |
