题目内容
1mol C与1mol 水蒸气反应生成1mol CO 和1mol H2,需要吸收 131.5kJ的热量.写出此反应的热化学方程式. .
考点:热化学方程式
专题:化学反应中的能量变化
分析:根据热化学方程式的书写方法来书写,注意反应吸放热的表示方法以及物质状态的标注.
解答:
解:1molC与1mol水蒸气反应生成1mol CO和1mol H2,吸收131.5kJ的热量,则热化学方程式为:C (S)+H2O (g)  CO (g)+H2 (g)△H=+131.5kJ?mol-1,
CO (g)+H2 (g)△H=+131.5kJ?mol-1,
故答案为:C (S)+H2O (g) CO (g)+H2 (g)△H=+131.5kJ?mol-1;
CO (g)+H2 (g)△H=+131.5kJ?mol-1;
 CO (g)+H2 (g)△H=+131.5kJ?mol-1,
CO (g)+H2 (g)△H=+131.5kJ?mol-1,故答案为:C (S)+H2O (g)
 CO (g)+H2 (g)△H=+131.5kJ?mol-1;
CO (g)+H2 (g)△H=+131.5kJ?mol-1;
点评:本题主要考查了热化学方程式的书写,需要注意的有:物质的状态、反应热的数值与单位,反应热的数值与化学方程式前面的系数成正比.

练习册系列答案
相关题目
下列叙述中正确的是( )
| A、在蔗糖中加入浓硫酸后出现发黑现象,说明浓硫酸具有脱水性 |
| B、向碘水中通入SO2,碘水褪色说明SO2具有漂白性 |
| C、蘸有浓硫酸的玻璃棒接近浓氨水瓶口有白烟产生 |
| D、某溶液加入BaCl2溶液,产生不溶于稀硝酸的白色沉淀,该溶液一定含有SO42- |
下列说法正确的是( )
A、 表示苯的分子结构,其中含有碳碳单键和双键,因此苯的性质与乙烯相似 表示苯的分子结构,其中含有碳碳单键和双键,因此苯的性质与乙烯相似 |
| B、乙烷中混有乙烯:在一定条件下通氢气,使乙烯转化为乙烷 而除去杂质 |
| C、苯在一定条件下能够和浓硝酸发生加成反应,生成硝基苯 |
| D、实验室鉴别己烯(C6H12)和苯,可以用酸性高锰酸钾溶液 |
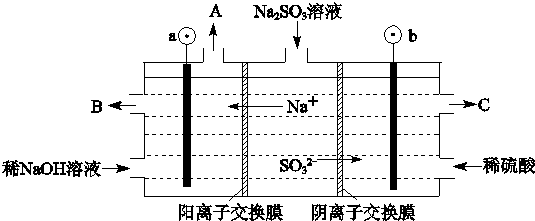
 .试回答:
.试回答: 和
和
