题目内容
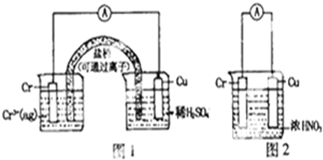
用如图装置进行实验(A为电流计),观察到现象:装置图1:Cu电极上产生大量的无色气泡;装置图2:Cu电极上无气泡产生,而Cr电极上产生大量气泡,则下列说法正确的是( )

| A、图1是电解池,图2是原电池 |
| B、两个电池中,电子均由Cr电极流向Cu电极 |
| C、图2中Cr电极可能被浓HNO3钝化成惰性电极 |
| D、由实验现象可知金属活动性:Cu>Cr |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:观察到图1装置铜电极上产生大量的无色气泡,说明图1中,Cr为负极,铜为正极,正极上析出氢气,而图2装置中铜电极上无气体产生,铬电极上产生大量气体,说明铜被氧化应为负极,正极上应是硝酸被还原生成二氧化氮气体,以此解答该题.
解答:
解:A.图1与图2中均没有外加电源,所以均为原电池装置,故A错误;
B.图1中Cr为负极,铜为正极,电子由Cr经导线流向Cu,图2中Cr为正极,Cu为负极,电子由Cu极经导线流向Cr,故B错误;
C.图2中Cr电极被浓HNO3钝化成惰性电极作正极,Cu失电子作负极,故C正确;
D.由图1根据原电池原理知金属铬的活动性比铜强,故D错误.
故选C.
B.图1中Cr为负极,铜为正极,电子由Cr经导线流向Cu,图2中Cr为正极,Cu为负极,电子由Cu极经导线流向Cr,故B错误;
C.图2中Cr电极被浓HNO3钝化成惰性电极作正极,Cu失电子作负极,故C正确;
D.由图1根据原电池原理知金属铬的活动性比铜强,故D错误.
故选C.
点评:本题综合考查原电池知识,侧重于学生的分析能力的考查,注意把握原电池的工作原理,答题时注意体会原电池电极的判断方法,难度中等.

练习册系列答案
相关题目
在一定温度下,将2.0mol PCl3和1.0mol Cl2通入一容积不变的密闭容器中,达到如下平衡:PCl3(g)+Cl2(g)?PCl5(g)测得平衡混合气PCl5为0.40mol;如果此时移走1.0mol PCl3和0.50mol Cl2,在温度不变时,重新达衡时PCl5的物质的量是( )
| A、0.40mol |
| B、0.20mol |
| C、小于0.20mol |
| D、大于0.20mol,小于0.40mol |
 往一体积不变的密闭容器中充入H2和I2,发生反应H2(g)+I2(g)?2HI(g);△H<0,当达到平衡后,t0时改变反应的某一条件,平衡图象如图,则下列说法正确的是( )
往一体积不变的密闭容器中充入H2和I2,发生反应H2(g)+I2(g)?2HI(g);△H<0,当达到平衡后,t0时改变反应的某一条件,平衡图象如图,则下列说法正确的是( )| A、容器内气体颜色变深,平均相对分子质量不变 |
| B、平衡不移动,混合气体密度增大 |
| C、H2转化率增大,HI平衡浓度变小 |
| D、t0时改变的条件是增压 |
下列颜色的变化中,不是因为发生化学反应而产生的是( )
| A、乙烯使酸性KMnO4溶液褪色 |
| B、甲烷与氯气混合光照后黄绿色变浅 |
| C、乙烯使溴的四氯化碳溶液褪色 |
| D、将苯滴入溴水中,振荡后水层接近无色 |
下列现象或事实可用同一原理解释的是( )
| A、氯化铵晶体和碘晶体加热都产生气体 |
| B、明矾和液氯都可用于处理生活用水 |
| C、漂白粉和过氧化钠都可用于漂白有色织物 |
| D、常温下,铁和铜分别放在浓硫酸中都无明显现象 |
下列操作达不到预期目的是( )
①石油分馏时把温度计插入液面以下
②用溴水除去乙烯中混有的SO2气体
③用乙醇与1mol/L的H2SO4混合共热到170℃制取乙烯
④将饱和食盐水滴入盛有电石的烧瓶中制乙炔.
①石油分馏时把温度计插入液面以下
②用溴水除去乙烯中混有的SO2气体
③用乙醇与1mol/L的H2SO4混合共热到170℃制取乙烯
④将饱和食盐水滴入盛有电石的烧瓶中制乙炔.
| A、①④ | B、③④ |
| C、②③④ | D、①②③ |
下列叙述中正确的是( )
| A、在蔗糖中加入浓硫酸后出现发黑现象,说明浓硫酸具有脱水性 |
| B、向碘水中通入SO2,碘水褪色说明SO2具有漂白性 |
| C、蘸有浓硫酸的玻璃棒接近浓氨水瓶口有白烟产生 |
| D、某溶液加入BaCl2溶液,产生不溶于稀硝酸的白色沉淀,该溶液一定含有SO42- |
 .试回答:
.试回答: