题目内容
某原电池的离子方程式是 Cu+2Fe3+=Cu2++2Fe2+,该原电池正确的组成是( )
| 正极 | 负极 | 电解质溶液 | |
| A. | Ag | Cu | AgNO3 |
| B. | Zn | Cu | FeCl3 |
| C. | C | Cu | FeCl3 |
| D. | Cu | Ag | Fe2(SO4)3 |
| A、A | B、B | C、C | D、D |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:原电池总反应离子方程式为:Cu+2Fe3+=Cu2++2Fe2+,Cu失去电子,为原电池的负极,正极为比Cu不活泼的金属或非金属,电解质为氯化铁或硫酸铁,以此来解答.
解答:
解:根据电池反应式知,负极上铜失电子发生氧化反应,正极上铁离子得电子发生还原反应,所以负极材料应该是铜,正极材料应该是不如铜活泼的金属或石墨,电解质溶液应该是氯化铁或硫酸铁都可,只有C符合.
故选C.
故选C.
点评:本题考查原电池,明确电池反应中元素的化合价变化为解答的关键,注意铁离子得电子分析电解质,注重基础知识的考查,题目难度不大.

练习册系列答案
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目
禁止运动员使用兴奋剂是2012绿色奥运的重要举措之一,如图是兴奋剂利尿酸的结构:关于它的说法正确的是( )
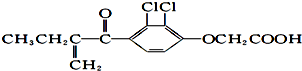

| A、利尿酸的化学式为:C13H14O4Cl2 |
| B、1mol 利尿酸最多可与4 mol H2发生反应 |
| C、利尿酸可使溴的四氯化碳溶液褪色 |
| D、利尿酸在一定条件下能发生消去反应 |
下列书写正确的是( )
| A、硫化钠水解:S2-+2H2O?H2S+2OH- |
| B、碳酸钠与醋酸溶液反应:CO32-+2H+=H2O+CO2↑ |
| C、HCO3-的电离:H2O+HCO3-?CO32-+H3O+ |
| D、NaHS在水中的电离:NaHS?Na++HS- HS-?H++S2- |
下列反应中既属于氧化还原反应,又属于吸热反应的是( )
A、C(石墨)=C(金刚石),在该反应进程中其能量变化如下图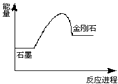 |
| B、Ba(OH)2?8H2O与NH4Cl反应 |
| C、灼热的碳与CO2反应 |
| D、甲烷在氧气中燃烧 |
某元素原子核外电子排布为:第二层上的电子数比第一层与第三层电子数之和的两倍还多2,该元素是( )
| A、Na | B、Mg | C、Al | D、Cl |
下列说法正确的是( )
| A、含有共价键的化合物一定是共价化合物 |
| B、不同元素原子形成的多原子分子中,含有的化学键只能是极性共价键 |
| C、非极性共价键只能存在于非金属单质或共价化合物中 |
| D、含有离子键的化合物一定是离子化合物 |
关于A(g)+2B(g)═3C(g)的化学反应,下列表示的反应速率最大的是( )
| A、v(A)=0.6mol/(L?min) |
| B、v(B)=1.2mol/(L?min) |
| C、v(C)=1.2mol/(L?min) |
| D、v(B)=0.03mol/(L?s) |