题目内容
某元素原子核外电子排布为:第二层上的电子数比第一层与第三层电子数之和的两倍还多2,该元素是( )
| A、Na | B、Mg | C、Al | D、Cl |
考点:原子结构与元素的性质
专题:原子组成与结构专题
分析:原子核外电子排布中,第一电子层排列2个电子、第二电子层排列8个电子,第二层上的电子数比第一层与第三层电子数之和的两倍还多2,设第三电子层电子数是x,则2(2+x)+2=8,据此解答.
解答:
解:原子核外电子排布中,第一电子层排列2个电子、第二电子层排列8个电子,第二层上的电子数比第一层与第三层电子数之和的两倍还多2,设第三电子层电子数是x,则2(2+x)+2=8,x=1,所以该原子第三电子层上有1个电子,则为Na元素,
故选A.
故选A.
点评:本题考查了原子结构和元素性质,熟悉原子结构及原子核外电子排布规律是解本题关键,再结合各个电子层上电子数之间的关系计算,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
某同学在实验室中进行如表实验:
以下结论正确的是( )
| 编号 | I | Ⅱ | Ⅲ |
| 实验 | 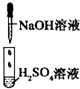 |
 |
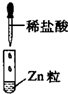 |
| 现象 | 没有明显变化,溶液仍为无色 | 有白色沉淀生成,溶液为蓝色 | 有无色气体放出 |
| A、I中混合前后溶液中各离子种类、个数均不变 |
| B、Ⅱ中反应前后溶液中Cu2+、Cl-浓度均未变 |
| C、Ⅱ中BaCl2替换为Ba(NO3)2溶液,发生的离子反应相同 |
| D、Ⅲ中发生的反应属于置换反应,不属于离子反应 |
下列方法中可以说明2HI(g)?H2(g)+I2(g)已达到平衡的是( )
| A、c(HI):c(H2):c(I2)=2:1:1时 |
| B、温度和体积一定时,混合气体的颜色不再改变 |
| C、单位时间内生成n mol H2的同时消耗2n mol HI |
| D、温度和体积一定时,容器内压强不再变化 |
下列说法正确的是( )
| A、增大压强,活化分子数增多 |
| B、升高温度,活化分子百分数增大 |
| C、使用催化剂能降低反应热 |
| D、加入反应物,使活化分子百分数增加,化学反应速率增大 |
下列各电离方程式中,书写正确的是( )
| A、H2S?2H++S2- |
| B、KHSO4?K++H++SO42- |
| C、Al(OH)3═Al3++3OH- |
| D、NaH2PO4═Na++H2PO4- |
下列物质的变化过程中,没有化学键断裂的是( )
| A、HCl溶解于水 |
| B、NaCl晶体的熔化 |
| C、干冰升华 |
| D、氯化铵的“升华” |