题目内容
3.微型纽扣电池在现代生活中有广泛应用,有一种银锌电池,其电极分别是Ag2O和Zn,电解质溶液为KOH溶液,电极反应式为:Zn+2 OH--2e-=ZnO+H2O Ag2O+H2O+2e-=2Ag+2OH-,总反应式为Ag2O+Zn=ZnO+2Ag,根据上述反应式,判断下列叙述中正确的是( )| A. | 在使用过程中,电池负极区溶液的pH增大 | |
| B. | 在使用过程中,电子由Ag2O经外电路流向Zn极 | |
| C. | Zn是负极,Ag2O是正极 | |
| D. | Zn极发生还原反应,Ag2O极发生氧化反应 |
分析 A.根据元素化合价变化知,Zn失电子而作负极,负极上OH-参加反应导致其浓度减小;
B.该原电池中,Zn是负极、Ag2O是正极,电子从负极沿导线流向正极;
C.电池反应中Zn元素化合价由0价变为+2价、Ag元素化合价由+1价变为0价,所以Zn是负极、Ag2O是正极;
D.失电子的物质发生氧化反应、得电子的物质发生还原反应.
解答 解:A.根据元素化合价变化知,Zn失电子而作负极,负极上OH-参加反应导致其浓度减小,溶液的碱性降低,pH减小,故A错误;
B.该原电池中,Zn是负极、Ag2O是正极,电子从负极Zn沿导线流向正极Ag2O,故B错误;
C.电池反应中Zn元素化合价由0价变为+2价、Ag元素化合价由+1价变为0价,所以Zn是负极、Ag2O是正极,负极上发生氧化反应、正极上发生还原反应,故C正确;
D.Zn失电子发生氧化反应、Ag2O得电子发生还原反应,故D错误;
故选C.
点评 本题考查化学电源新型电池,侧重考查分析判断能力,明确元素化合价变化与电极关系是解本题关键,知道各个电极上反应类型、电子及电流流向,题目难度不大.

练习册系列答案
相关题目
15.下列事实能说明甲酸(HCOOH)属于弱酸的是( )
①1mol•L-1 HCOOH溶液的pH=2
②甲酸能与水以任意比互溶
③20mL 1mol•L-1HCOOH与20mL 1mol•L-1NaOH恰好中和
④HCOONa溶液的pH>7.
①1mol•L-1 HCOOH溶液的pH=2
②甲酸能与水以任意比互溶
③20mL 1mol•L-1HCOOH与20mL 1mol•L-1NaOH恰好中和
④HCOONa溶液的pH>7.
| A. | ①② | B. | ② | C. | ③④ | D. | ①④ |
11.现有一由Na2SO4、Na2SO3、Na2S组成的混和物,经测定硫的质量分数为2 5.6%,则此混合物中氧元素的质量分数应为( )
| A. | 37.6% | B. | 36.8% | C. | 25.6% | D. | 51.2% |
8.下列说法中正确的是( )
| A. | 非金属原子间以共价键结合的物质都是共价化合物 | |
| B. | 由不同原子所形成的纯净物一定是化合物 | |
| C. | 含有金属元素的离子不一定是阳离子 | |
| D. | 离子化合物一定能导电 |
15.电解普通水(H2O)和重水(D2O)的混合物,通电一段时间后,两极共生成气体18.5g,其体积为33.6L(标况下),在所生成的气体中重氢和普通氢的原子个数比为( )
| A. | 2:3 | B. | 2:5 | C. | 1:2 | D. | 1:3 |
12.能发生消去反应,生成物中存在同分异构体的是( )
| A. | 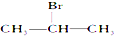 | B. | 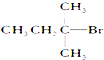 | C. | 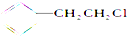 | D. | CH3CH2Br |
13.设NA为阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 0.1 mol ${\;}_{8}^{16}$OD- 离子含有的质子、中子数均为1.0NA | |
| B. | 含有4.6 g钠元素的过氧化钠和氧化钠的混合物中,所含离子总数为0.3NA | |
| C. | 3.6 g石墨中,含有共价键数为0.3NA | |
| D. | 标准状况下,4.48 L己烷含有的分子数为0.2NA |