题目内容
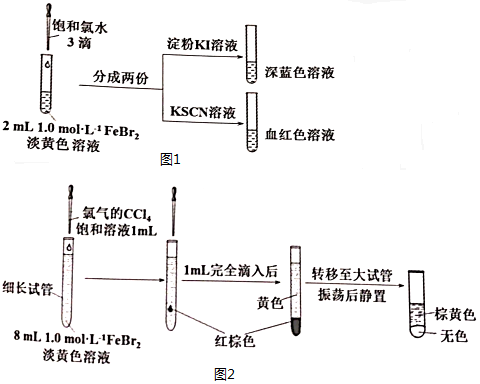
11.下列化学反应先后顺序判断正确的是( )| A. | 在含有等物质的量的FeBr2、FeI2的溶液中,缓慢通入氯气:I-、Br-、Fe2+ | |
| B. | 在含有等物质的量的OH-、CO32-、SO32-的溶液中加入稀盐酸:OH-、SO32-、CO32- | |
| C. | 在含有等物质的量的Fe3+、Cu2+的溶液中加入铁粉:Cu2+、Fe3+ | |
| D. | 在含有等物质的量的H+、Al3+的溶液中,逐滴加入NaOH溶液:H+、Al3+、Al(OH)3 |
分析 A、溶液中离子的还原性强弱顺序是I->Fe2+>Br-,向溶液中滴加过量氯水时发生的反应分别为:2I-+Cl2=2Cl-+I2、2Fe2++Cl2=2Fe3++2Cl-、Cl2+2Br-=2Cl-+Br2;
B、亚硫酸的酸性强于碳酸,所以碳酸根离子结合氢离子的能力强于亚硫酸根离子;
C、铁离子的氧化性强于铜离子;
D、氢氧化铝是两性化合物,所以铝离子结合氢氧根离子,生成氢氧化铝,氢氧化铝再与氢氧化钠反应生成偏铝酸钠.
解答 解:A、溶液中离子的还原性强弱顺序是I->Fe2+>Br-,向溶液中滴加过量氯水时发生的反应分别为:2I-+Cl2=2Cl-+I2、2Fe2++Cl2=2Fe3++2Cl-、Cl2+2Br-=2Cl-+Br2,所以参与反应的离子先后顺序为:I-、Fe2+、Br-,故A错误;
B、亚硫酸的酸性强于碳酸,所以碳酸根离子结合氢离子的能力强于亚硫酸根离子,所以在含有等物质的量的OH-、CO32-、SO32-的溶液中加入稀盐酸,反应先后顺序OH-、CO32-、SO32-,故B错误;
C、铁离子的氧化性强于铜离子,所以在含有等物质的量的Fe3+、Cu2+的溶液中加入铁粉,反应的先后顺序Fe3+、Cu2+,故C错误;
D、氢氧化铝是两性化合物,所以铝离子结合氢氧根离子,生成氢氧化铝,氢氧化铝再与氢氧化钠反应生成偏铝酸钠,所以在含有等物质的量的H+、Al3+的溶液中,逐滴加入NaOH溶液,反应先后顺序H+、Al3+、Al(OH)3,故D正确;
故选D.
点评 本题考查微粒反应的先后顺序,特别氧化还原反应先后顺序、氧化性和还原性强弱比较等知识,试题综合性较强,难度较大,明确反应过程及反应原理为解题关键.

练习册系列答案
相关题目
20.下列关于氯气的叙述正确的是( )
| A. | 钠在氯气中燃烧产生白色烟雾 | |
| B. | 红热的铜丝可以在氯气中燃烧,产生棕黄色烟雾 | |
| C. | 纯净的氢气可以在氯气中安静地燃烧,发出苍白色火焰 | |
| D. | 氯气可用于漂白,这是氯气的漂白作用 |
1.下列关于油脂的叙述正确的是( )
| A. | 油脂均为固体 | |
| B. | 油脂在体内直接氧化产生热量 | |
| C. | 多吃动物脂肪比多吃植物油有利 | |
| D. | 有些脂肪酸是人体必需的,但在人体内却不能合成;脂肪中必需脂肪酸的含量越高,其营养价值越高 |
6.下列各化合物的命名中正确的是( )
| A. | CH2=CH-CH=CH2 1,4-丁二烯 | B. |  3-丁醇 3-丁醇 | ||
| C. |  甲基苯酚 甲基苯酚 | D. |  2-甲基丁烷 2-甲基丁烷 |
16.纤维分天然纤维和化学纤维,化学纤维又可分为合成纤维和人造纤维,下列材料中,主要成分属于合成纤维的是( )
①纯棉②涤纶③人造羊毛④黏胶纤维⑤醋酸纤维⑥羊毛.
①纯棉②涤纶③人造羊毛④黏胶纤维⑤醋酸纤维⑥羊毛.
| A. | ①②⑥ | B. | ③⑥ | C. | ②③ | D. | ①②③④⑤⑥ |
3.化学与生产、生活、科技等密切相关,下列说法不正确的是( )
| A. | 加大清洁能源的开发利用,提髙资源的利用率 | |
| B. | 研发使用高效催化剂,可提高反应中原料的转化率 | |
| C. | 用K2FeO4取代Cl2处理饮用水,可杀菌消毒,还能沉降水中的悬浮物 | |
| D. | 用沼气、太阳能、风能等新型能源代替化石燃料 |
1.加入Al能产生H2的溶液中一定能大量共存的是( )
| A. | K+、Na+、Br-、SO42- | B. | Na+、Ba2+、ClO-、Cl- | ||
| C. | Ca2+、Cl-、HCO3-、K+ | D. | NH4+、K+、OH-、SO42- |