题目内容
组成为
X的元素在周期表中的位置是( )
39 19 |
| A、第3周期第0族 |
| B、第4周期第ⅠA族 |
| C、第3周期第ⅠA族 |
| D、第3周期第ⅦA族 |
考点:元素周期表的结构及其应用
专题:元素周期律与元素周期表专题
分析:元素符号的左上角表示质量数,左下角表示质子数,质子数=核电荷数=原子序数,所以
X的原子序数为19,该元素原子的原子核外电子排布为: ,据此判断该元素在周期表中的位置.
,据此判断该元素在周期表中的位置.
39 19 |
 ,据此判断该元素在周期表中的位置.
,据此判断该元素在周期表中的位置.解答:
解:
X的质量数为39、质子数=原子序数=19,根据原子核外电子排布规律可知,该元素的原子结构示意图为: ,
,
所以该元素位于周期表中第4周期第ⅠA族,
故选B.
39 19 |
 ,
,所以该元素位于周期表中第4周期第ⅠA族,
故选B.
点评:本题考查了元素符号的表示方法、原子结构与物质的关系,题目难度不大,试题侧重基础知识的考查,注意掌握原子结构与元素周期表的关系,明确原子核外电子排布规律.

练习册系列答案
相关题目
下列原子的电子排布式能表示基态原子的电子排布式的是( )
| A、[Ne]3s13p3 |
| B、[Ar]3d64s1 |
| C、[Ar]3d64s2 |
| D、[Ne]3s23p63d5 |
在强酸性无色透明溶液中,下列各组离子能大量共存的是( )
| A、Cu2+、K+、Cl-、NO3- |
| B、Ag+、Na+、Cl-、NO3- |
| C、Mg2+、Al3+、SO42-、Cl- |
| D、Ba2+、NH4+、Cl-、HCO3- |
短周期元素甲、乙、丙、丁、戊五种元素在元素周期表中的位置如下图所示,其中戊是同周期中原子半径最小的元素.下列有关判断正确的是( )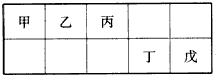

| A、最外层电子数:甲>乙>丙>丁>戊 |
| B、简单离子的离子半径:戊>丁>丙 |
| C、含有丁元素的酸有多种 |
| D、乙的氢化物多种多样,丙、丁、戊的氢化物各有一种 |
区分胶体与溶液的依据是( )
| A、分散质直径大小 |
| B、是否有丁达尔现象 |
| C、是否稳定 |
| D、分散质粒子是否带电 |
针对如图所示乙醇分子结构,下述关于乙醇在各种化学反应中化学键断裂情况的说法不正确的是( )
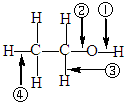

| A、与醋酸、浓硫酸共热时,②键断裂 |
| B、与金属钠反应时,①键断裂 |
| C、与浓硫酸共热至170℃时,②、④键断裂 |
| D、在Ag催化下与O2反应时,①、③键断裂 |
