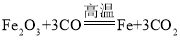【题目】下表是熟石灰与硝酸钾在不同温度下的溶解度,下列说法正确的是( )
温度/℃ | 0 | 20 | 40 | 100 |
熟石灰溶解度/g | 0.173 | 0.165 | 0.121 | 0.076 |
硝酸钾溶解度/g | 13.3 | 31.6 | 63.9 | 246 |
A.20℃时,将熟石灰的饱和溶液温度升高会变为不饱和溶液
B.100℃时,将硝酸钾的饱和溶液冷却至室温会析出晶体,但溶液仍饱和
C.20℃时,熟石灰溶液的溶质质量分数一定小于硝酸钾溶液的溶质质量分数
D.20℃时,将100克硝酸钾固体投入100克水中,所得溶液的溶质质量分数为50%
【题目】某矿样含有大量的 CuS 及少量其它不溶于水、不与酸反应的杂质。实验室中 以该矿样为原料制备CuSO4·5H2O晶体,并最终制取碱式碳酸铜。
I. 制备CuSO4·5H2O晶体
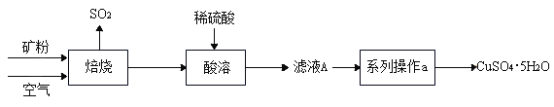
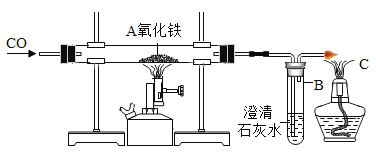
(1)矿样中 CuS 在空气中焙烧生成了 CuO,反应方程式为___;
(2)在实验室中,欲用 98%、密度1.84g/cm3的浓硫酸配制500 g质量分数10%的稀硫酸, 需要的仪器除量筒、烧杯、玻璃棒外,还有___。稀释过程___(填“放热”或“吸 热”)。
(3)若在实验室中完成系列操作 a,主要步骤为____→降温结晶→____→洗涤→低温干燥。(以上选填字母)
II. 制备碱式碳酸铜
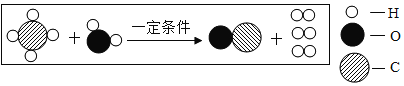
(4)实验室制备碱式碳酸铜的反应原理为:(将短线上的物质补充完整)
![]() ____↑+2Na2SO4。
____↑+2Na2SO4。
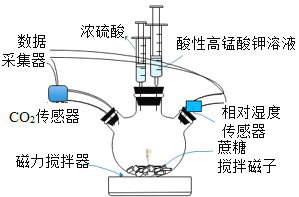
(5)分别取 50mL一定浓度的CuSO4溶液与Na2CO3 溶液混合,发现反应后烧杯底部出现大量蓝绿色沉淀。查阅资料得知蓝绿色沉淀中混有难溶于水的碱式硫酸铜[Cu2(OH)2SO4]。为确定该物质,经过滤、洗净后取少量固体于试管中,加入足量稀盐酸将固体完全溶解,再滴加几滴____溶液出现白色沉淀,证明含有Cu2(OH)2SO4。
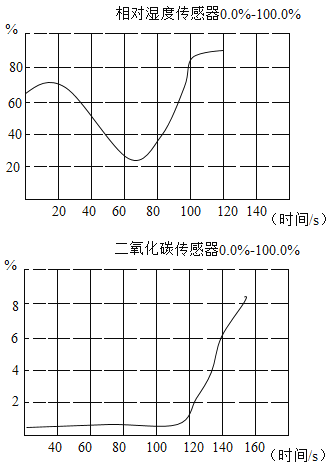
(6)按最佳配比进行实验制备碱式碳酸铜,反应过程中测得数据如下:
温度/℃ | 60 | 65 | 75 | 80 | 90 |
沉淀量/g | 1.295 | 1.303 | 1.451 | 1.340 | 1.292 |
据此分析制备反应控制的适宜温度是____,推测 90°C固体较少的原因是____。
(7)查阅资料可知碱式碳酸铜的组成有多种,可用xCu(OH)2yCuCO3表示。某小组利用 以下装置测定某碱式碳酸铜样品的组成:(资料:碱式碳酸铜受热分解成三种常见的氧化物;碱石灰是氧化钙与氢氧化钠的混合物)
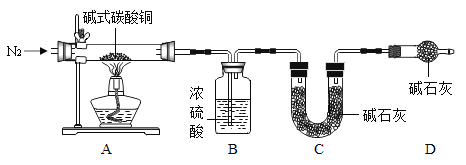
①加热时持续通入N2的目的是____,D 装置的作用是____。
②称取 32.0g 样品,充分反应后得到 24.0g 残留物,B 增重 3.6g,C 增重 4.4g。该样品的化学式为____。若对调 B 和 C 装置的位置,____(填“能”或“不能”)测算出该样品的化学式。
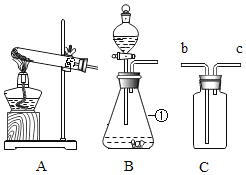
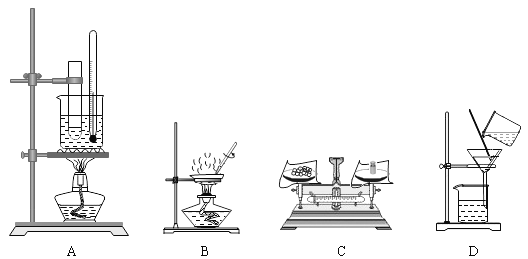
【题目】(1)实验室常用过氧化氢溶液与二氧化锰制取氧气,选用的发生装置为____填字母), 反应原理用化学方程式表示为____,二氧化锰在反应前后____和____保持不变。 收集氧气可以用____ (填“向上”或“向下”)排空气法,检验氧气已经收集满的方法是____。
(2)研究小组继续探究影响过氧化氢分解速度的相关因素,做如下实验:

(实验 1)研究不同催化剂对过氧化氢分解速度的影响
在两只烧杯中,分别加入 10mL 约 10%的过氧化氢溶液和 5 滴洗洁精,再向其中分别 加入 4mL 质量分数为 10%的 KI、酵母液,实验结果如下表所示。
物质 | H2O2 | 现象 |
10%KI | 10% | 立即产生淡黄色气泡,溶液变成黄色,48s 后泡沫到达烧杯顶端 |
10%酵母 | 10% | 立即产生白色气泡,10s 后泡沫到达烧杯顶端 |
生活中洗洁精可清除油污,其原理是____(填“溶解”、“乳化”或“化学反应”)。
此实验中是便于形成泡沫观察反应的速度。
据表分析,加入 KI 的烧杯中变黄可能是产生了碘单质,可以通过加入____(填物质名称)后变蓝色检验确认。酵母使过氧化氢分解速度明显加快,继续研究。
(实验 2)研究不同浓度酵母液对双氧水分解速度的影响
在五只烧杯中,分别加入约 10%过氧化氢溶液和5滴洗洁精,再分别加入4mL 质量 分数为 2%、5%、10%、15%的酵母液,实验结果下表所示
酵母液 | H2O2 | 现象 |
2% | 10% | 产生白色气泡,1min25s 后泡沫到达烧杯顶端 |
5% | 10% | 产生白色气泡,42s 后泡沫到达烧杯顶端 |
10% | 10% | 立即产生白色气泡,10s 后泡沫到达烧杯顶端 |
15% | 10% | 立即产生白色气泡,8s 后泡沫到达烧杯顶端 |