题目内容
【题目】如图是实验室制取气体的部分装置,请根据实验装置(部分固定装置已省略)回答问题:
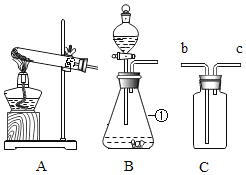
(1)仪器①的名称为__。
(2)实验室用高锰酸钾制备O2,反应的化学方程式为____,应选用的发生装置为__(填序号),若利用装置C通过排水法收集O2并测定体积,则应在__端(填“b”或“c”)连接一个量筒。
(3)实验室制取氢气应选用的药品是_____(填名称),若要能够控制反应的速率,则应选择的发生装置为__(填序号)。
【答案】锥形瓶 2KMnO4![]() K2MnO4+MnO2+O2↑ A b 锌粒和稀硫酸 B
K2MnO4+MnO2+O2↑ A b 锌粒和稀硫酸 B
【解析】
(1)据图可知仪器①的名称为锥形瓶;
(2)如果用高锰酸钾制氧气就需要加热,高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,反应的化学方程为2KMnO4![]() K2MnO4+MnO2+O2↑;氧气密度小于水,若利用装置C通过排水法收集O2并测定体积,则应在b连接一个量筒;
K2MnO4+MnO2+O2↑;氧气密度小于水,若利用装置C通过排水法收集O2并测定体积,则应在b连接一个量筒;
(3)实验室是用锌粒和稀硫酸在常温下反应制氢气的,若要能够控制反应的速率,则应选择的发生装置为B。

【题目】某矿样含有大量的 CuS 及少量其它不溶于水、不与酸反应的杂质。实验室中 以该矿样为原料制备CuSO4·5H2O晶体,并最终制取碱式碳酸铜。
I. 制备CuSO4·5H2O晶体
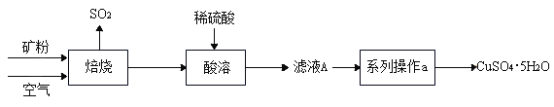
(1)矿样中 CuS 在空气中焙烧生成了 CuO,反应方程式为___;
(2)在实验室中,欲用 98%、密度1.84g/cm3的浓硫酸配制500 g质量分数10%的稀硫酸, 需要的仪器除量筒、烧杯、玻璃棒外,还有___。稀释过程___(填“放热”或“吸 热”)。
(3)若在实验室中完成系列操作 a,主要步骤为____→降温结晶→____→洗涤→低温干燥。(以上选填字母)
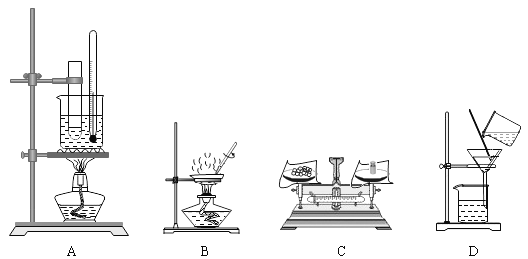
II. 制备碱式碳酸铜
(4)实验室制备碱式碳酸铜的反应原理为:(将短线上的物质补充完整)
![]() ____↑+2Na2SO4。
____↑+2Na2SO4。
(5)分别取 50mL一定浓度的CuSO4溶液与Na2CO3 溶液混合,发现反应后烧杯底部出现大量蓝绿色沉淀。查阅资料得知蓝绿色沉淀中混有难溶于水的碱式硫酸铜[Cu2(OH)2SO4]。为确定该物质,经过滤、洗净后取少量固体于试管中,加入足量稀盐酸将固体完全溶解,再滴加几滴____溶液出现白色沉淀,证明含有Cu2(OH)2SO4。
(6)按最佳配比进行实验制备碱式碳酸铜,反应过程中测得数据如下:
温度/℃ | 60 | 65 | 75 | 80 | 90 |
沉淀量/g | 1.295 | 1.303 | 1.451 | 1.340 | 1.292 |
据此分析制备反应控制的适宜温度是____,推测 90°C固体较少的原因是____。
(7)查阅资料可知碱式碳酸铜的组成有多种,可用xCu(OH)2yCuCO3表示。某小组利用 以下装置测定某碱式碳酸铜样品的组成:(资料:碱式碳酸铜受热分解成三种常见的氧化物;碱石灰是氧化钙与氢氧化钠的混合物)
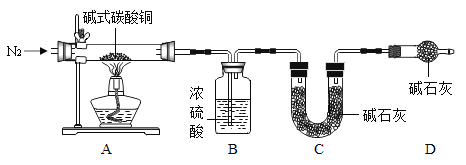
①加热时持续通入N2的目的是____,D 装置的作用是____。
②称取 32.0g 样品,充分反应后得到 24.0g 残留物,B 增重 3.6g,C 增重 4.4g。该样品的化学式为____。若对调 B 和 C 装置的位置,____(填“能”或“不能”)测算出该样品的化学式。
【题目】下表给出了某些金属的信息。如表给出了某些金属的信息。
每吨金属在2020年4月的价格(元) | 地壳中的含量(%) | |
铝 | 16000 | 7.73 |
铂 | 305000000 | 0.0000001 |
铁 | 4500 | 4.75 |
金 | 320000000 | 0.0000001 |
(1)依据表中信息解释,金和铂均很昂贵的原因是________________。
(2)工业上用含铝、铁的矿石制取铝和铁。
①铝抗腐蚀性强的原因是_________________________。
②将熔融的氧化铝通电分解,可获得铝和另一种单质。反应的化学方程式是______________。
③根据化学方程式计算,用赤铁矿(主要成分为Fe2O3)炼铁,若要得到112t铁,理论上需要Fe2O3的质量为多少t?_____________