题目内容
【题目】下表是熟石灰与硝酸钾在不同温度下的溶解度,下列说法正确的是( )
温度/℃ | 0 | 20 | 40 | 100 |
熟石灰溶解度/g | 0.173 | 0.165 | 0.121 | 0.076 |
硝酸钾溶解度/g | 13.3 | 31.6 | 63.9 | 246 |
A.20℃时,将熟石灰的饱和溶液温度升高会变为不饱和溶液
B.100℃时,将硝酸钾的饱和溶液冷却至室温会析出晶体,但溶液仍饱和
C.20℃时,熟石灰溶液的溶质质量分数一定小于硝酸钾溶液的溶质质量分数
D.20℃时,将100克硝酸钾固体投入100克水中,所得溶液的溶质质量分数为50%
【答案】B
【解析】
A、氢氧化钙的溶解度随着温度的升高而减小,20℃时,将熟石灰的饱和溶液温度升高,溶解度减小,有氢氧化钙析出,仍为不饱和溶液,故选项说法错误;
B、硝酸钾的溶解度随着温度的降低而减小,100℃时,将硝酸钾的饱和溶液冷却至室温会析出晶体,溶液仍为饱和溶液,故选项说法正确;
C、选项没有指明溶液是否饱和,20℃时,熟石灰溶液的溶质质量分数不一定小于硝酸钾溶液的溶质质量分数,故选项说法错误;
D、20℃时,硝酸钾的溶解度为31.6g,20℃时,将100克硝酸钾固体投入100克水中,最多只能溶解31.6g,所得溶液中溶质质量分数为![]() ×100%<31.6%,故选项说法错误。
×100%<31.6%,故选项说法错误。
故选B。

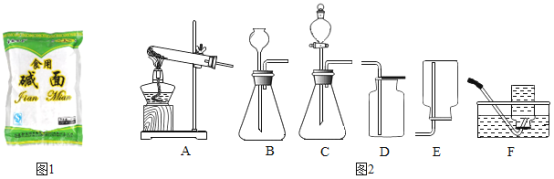
【题目】小明同学在超市里看到“食用碱面”(如图1所示),他想知道该“食用碱面”的成分,请教老师后得知它的主要成分是一种钠盐。
(作出猜想)小明及其他同学猜想其主要成分可能是:
①Na2SO4 ②NaCl ③Na2CO3 ④NaHCO3
(查阅资料)(1)氯化钡溶液与碳酸氢钠溶液不反应。
(2)碳酸氢钠溶液呈碱性。
小明与同学们进行如下实验来确认该“食用碱面”的主要成分。
(进行实验)取适量该“食用碱面”于试管中,加入蒸馏水使之完全溶解,把所得溶液分成两等份。
实验操作 | 实验现象 | 实验结论 |
实验①:在第一份溶液中加入氯化钡溶液 | _____ | 猜想①正确 |
实验②:在第二份溶液中加入_____ | 有气泡产生 | 猜想_____正确 |
(交流讨论)
(1)同学们经过讨论,发现仅仅通过实验①不能得出该“食用碱面”的主要成分是Na2SO4,也可能是Na2CO3,原因是_____(用化学方程式表示)。
(2)同学们通过对实验①②的分析得出该“食用碱面”的主要成分是Na2CO3,理由是_____。
(3)有同学认为把酚酞溶液滴入该“食用碱面”的溶液中,溶液变红,就可得出该“食用碱面”的主要成分是Na2CO3.这种说法对吗?并请说明原因:_____。
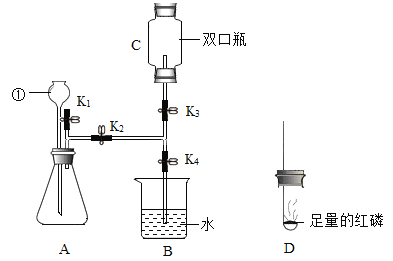
(拓展应用)已知Na2CO3与稀盐酸反应非常剧烈。实验室欲用Na2CO3固体和稀盐酸制取并收集二氧化碳,你选择的装置最好是_____(选填图2中装置序号)。
【题目】某校化学兴趣小组对如何鉴别生活中的苏打(Na2CO3)和小苏打(NaHCO3),进行了下列探究: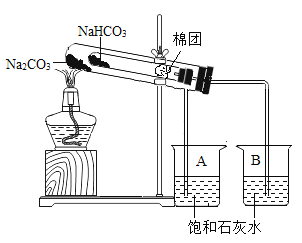
(查阅资料)
①相同条件下,碳酸钠溶液比碳酸氢钠溶液的碱性强;
②270℃时,NaHCO3会完全分解生成二氧化碳、水及一种白色固体,而Na2CO3不易分解:
③常见的碳酸盐中,只有碳酸钠、碳酸钾和碳酸铵溶于水,其它碳酸盐大多不溶于水。
(实验探究)
(1)充分加热后,A、B两烧杯中的现象分别为__、__、__,由此可得出的结论是__。
(2)现有浓度相同的Na2CO3与NaHCO3溶液,充分利用所学知识和资料,你认为区分二者最简单的方法是__。
A 加热 B 用pH试纸测溶液pH C 滴加稀盐酸
(反思与评价)
(1)常用小苏打治疗轻度胃酸过多的病人,原因是___(用化学方程式表示)。
(2)检验碳酸钠粉未中是否含有碳酸氢钠的方法是____。
(拓展延伸)该兴趣小组同学认为,充分加热NaHCO3后的白色固体产物可能是NaOH或Na2CO3。
(1)他们猜想的依据是_____。
(2)设计实验检验反应后的固体产物是NaOH还是Na2CO3,并完成下表(限选试剂及仪器:稀盐酸、氯化钡溶液、澄清石灰水、酚酞试液、蒸馏水、试管、胶头滴管)。
序号 | 实验操作 | 实验现象 | 实验结论 |
① | 取少量加热后的固体产物于试管A中,加入适量蒸馏水并充分振荡溶解,再加入足量____,振荡,静置 | 产生白色沉淀 | 产物中含有Na2CO3 |
② | 取操作①后的上层清液于试管B中,滴加_____ | _____ | 产物中不含NaOH |