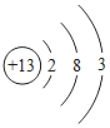【题目】某实验学校初三兴趣小组利用如下装置(部分固定装置已略去)。制备氮化钙,并探究其化学式
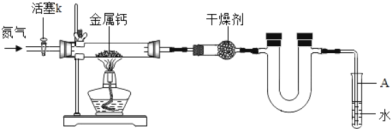
(1)反应过程中末端导管必须插入试管A的水中,目的是_____。
(2)制备氮化钙的操作步骤是:①打开活塞k并通入N2;②点燃酒精灯,进行反应;③反应结束后,_____;④拆除装置,取出产物。
(3)数据记录如下:
空硬玻璃管质量m0/g | 硬玻璃管与钙的质量m1/g | 硬玻璃管与产物的质量m2/g |
114.8 | 120.8 | 122.2 |
①计算得到化学式(实验式)CaxN2,其中x=_____。
②若通入的N2中混有少量O2,如上计算得到的x的值_____ (填写“偏大”、“偏小”、“不变”),判断依据是_____。
【题目】一碳化学是以分子中只含一个碳原子的化合物(如CO、CH4等)为原料来合成一系列化工原料和燃料的化学。
(1)工业上用天然气和水蒸气在高温条件下发生反应,得到CO和H2,该反应的化学方程式为_____,得到的CO和H2的混合气被称为合成气,合成气在工业上可用于合成一系列化工原料和新型燃料,还可用于冶炼某些金属。
(2)某他学兴趣小组的同学在实验室模拟了合成气的制备,并设计实验验证合成气的还原性。
I.用甲烷和水蒸气在高温条件下反应得到合成气。根据(1)中所写的化学方程式。合成气中CO和H2的质量比为_____。
Ⅱ.用合成气还原足量氧化铜。实验装置如图所示:

(设计买验步骤)
①连接好装置并检查气密性。
②装入药品,通入一段时间合成气。
③分别称量装置D、E的质量。
④缓缓通入合成气,加热装置C,使其充分反应。
⑤停止加热,继续通入合成气至恢复到室温。
⑥再次分别称量装置D、E的质量。
(完善实验设计)经过讨论同学们认为,装置E后还应添加一个酒精灯,并在实验步骤_____(填实验步骤的序号)中点燃(点燃前应对气体验纯)。
(进行实验)该小组的同学按上述步骤进行实验,并记录了实验现象和数据:
①装置C中出现_____色物质。
②称量数据如表所示。
装置D的质量 | 装置E的质量 | |
反应前 | 292.4g | 198.2g |
反应后 | 296.0g | 201.5g |
(现象分析和数据处理)
①甲同学根据装置C中的现象,认为是合成气中的CO和H2还原了CuO。
②乙同学通过对上表数据的分析,推测除了CO和H2以外,制得的合成气中可能还有未反应的CH4,且CH4也还原了CuO.试通过计算说明他的推测依据_____。
③丙同学提出,实验步骤⑤中通入的气体会带走装置E中的部分水蒸气,使实验产生误差。你认为该误差对乙同学的推测结果是否有影响?_____(选填“是”或“否”,并说明理由)。
(拓展探究)该小组同学对于CH4是否真的能够还原氧化铜提出了质疑并进行探究。
查阅资料:甲烷具有还原性,可以还原氧化铜,生成CO2和H2O;白色的无水硫酸铜遇水会变成蓝色。
实验设计:该小组同学拟用纯净的甲烷气体和如下装置进行实验。

①如图装置F中盛放的试剂名称是_____。
②如图装置的正确连接顺序是_____(填字母,且每套装置限用一次)。
(实验反思)除了可能是CH4也还原了CuO外,出现上表数据关系还可能是因为_____(写出一个原因,并说明理由)。