10.现有一包白色粉末,可能含有NaCl、Na2SO4、Na2CO3、CuCl2、CaCl2中的一种或几种物质.取少量该白色粉末,加水溶解后得到无色透明溶液,向所得溶液中加入足量Ba(NO3)2溶液后,产生白色沉淀,加入足量稀硫酸溶液,沉淀全部溶解.根据上述操作及现象,下列说法中一定正确的是( )
| A. | 原粉末中一定有Na2SO4、Na2CO3 | |
| B. | 原粉末中可能有NaCl | |
| C. | 原粉末中一定没有CuCl2、Na2SO4、CaCl2 | |
| D. | 原粉末中只有Na2CO3一种物质 |
9.只用一种试剂就能将Na2CO3、NH4Cl、NaCl 三种溶液区分开来的是( )
| A. | 澄清石灰水 | B. | CaCl2溶液 | C. | NaOH溶液 | D. | 稀盐酸 |
8.小明同学为了测定纯碱样品(碳酸钠与氯化钠的混合物)中碳酸钠的质量分数,取样品13.9g放入烧杯中,将60g质量分数为14.6%的稀盐酸分6次加入该样品中,充分反应后,测得反应生成气体的质量(m)数据如下表所示.
根据题目回答下列问题:
(1)纯碱样品完全反应后,生成CO2的质量为4.4g.
(2)请在坐标图中画出反应生成气体的质量(m)随稀盐酸质量变化的曲线.

(3)样品中碳酸钠的质量分数为76.3%(计算结果保留0.1%)
(4)求恰好完全反应所得溶液中溶质的质量分数.(请写出计算过程)
| 实验次数 | 第第1次次 | 第2次 | 第3次 | 第4次 | 第5次 | 第6次 |
| 加入稀盐酸质量(g) | 10 | 10 | 10 | 10 | 10 | 10 |
| 产生的气体质量(g) | 0.88 | 1.76 | 2.64 | 3.52 | 4.4 | 4.4 |
(1)纯碱样品完全反应后,生成CO2的质量为4.4g.
(2)请在坐标图中画出反应生成气体的质量(m)随稀盐酸质量变化的曲线.

(3)样品中碳酸钠的质量分数为76.3%(计算结果保留0.1%)
(4)求恰好完全反应所得溶液中溶质的质量分数.(请写出计算过程)
7.已知水的沸点随压强的减少而减低.现有如图所示实验装置,夹子开始处于关闭状态.将滴管中的氢氧化钠溶液滴入试管②与气体B充分反应后,打开夹子,发现试管①内的水立刻沸腾.则液体A和气体B的组合可能是( )

0 167163 167171 167177 167181 167187 167189 167193 167199 167201 167207 167213 167217 167219 167223 167229 167231 167237 167241 167243 167247 167249 167253 167255 167257 167258 167259 167261 167262 167263 167265 167267 167271 167273 167277 167279 167283 167289 167291 167297 167301 167303 167307 167313 167319 167321 167327 167331 167333 167339 167343 167349 167357 211419

| A. | A为氯化钙溶液,B为二氧化碳气体 | |
| B. | A为氢氧化钠溶液,B为氯化氢气体 | |
| C. | A为氢氧化钙溶液,B为一氧化碳气体 | |
| D. | A为稀硫酸溶液,B为氢气气体 |
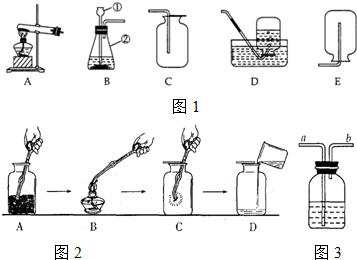
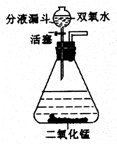 过氧化氢俗称双氧水,常温下是一种无色液体,它与二氧化锰混合后能迅速释放出氧气.此反应中二氧化锰作催化剂.在实验室中可用如图所示装置制取氧气.
过氧化氢俗称双氧水,常温下是一种无色液体,它与二氧化锰混合后能迅速释放出氧气.此反应中二氧化锰作催化剂.在实验室中可用如图所示装置制取氧气. 如图化学反应的溶液颜色变化体现了“魔法世界,魅力化学”.请回答:
如图化学反应的溶液颜色变化体现了“魔法世界,魅力化学”.请回答: 如图所示是X,Y,Z三种固体物质的溶解度曲线,看图回答下列问题:
如图所示是X,Y,Z三种固体物质的溶解度曲线,看图回答下列问题: