8.按照一定的依据把物质进行分类,是我们认识物质的组成、结构、性质和用途的便捷途径.小明同学在家中建立了小小化学实验室,他收集了许多物质,其中有:①纯碱;②生石灰;③酒精;④熟石灰;⑤尿素CO(NH2)2;⑥铜;⑦石墨;⑧氧化铁.⑨冰醋酸.对上述物质的分类不正确的是( )
| A. | 属于有机物的有③⑤⑨ | B. | 属于碱的有①④ | ||
| C. | 属于氧化物的有②⑧ | D. | 属于单质的有⑥⑦ |
7.下列说法中正确的是( )
| A. | pH>7的溶液一定是碱溶液 | |
| B. | 能电离出氢离子的化合物是酸 | |
| C. | 金属有良好延展性、可锻性,非金属单质材料中塑料具良好的可锻性 | |
| D. | 有机化合物都含有碳元素,含有碳元素的化合物不一定是有机化合物 |
6.实验室用氯酸钾和二氧化锰制取氧气,加热一段时间后剩余固体混合物10g,继续加热至完全反应后固体变为4.985g,再将固体加水充分溶解、过滤、干燥得到1.26g黑色固体.求10g剩余固体混合物中氯元素的质量分数为( )
| A. | 13.5% | B. | 17.75% | C. | 35.5% | D. | 42.6% |
5.2012年2月16日央视《焦点访谈》播出《打破钢锅问到底》,报道:苏泊尔81个规格炊具被认定为不合格产品,四大类包括汤锅、蒸锅、奶锅、水壶.钢锅锰含量高出国标近4倍,可致帕金森病.
(1)金属锰也是一种重金属,在我们人体或一些动物体内经常会检测到多种重金属离子的存在,进而危害我们的健康,这是为什么?金属离子可通过食物链在生物体内大量富集.
(2)某同学对金属锰、金属镁、金属铜的金属活泼性情况进行简单的实验如下,将金属锰分别放入硫酸镁和硫酸铜溶液中,分别记录现象如下:
由以上实验可知三种金属的活动性顺序是镁>锰>铜.
(3)常见金属中有些能和水或水蒸汽发生反应,请根据金属活动性顺序和表中的已知信息回答:
根据金属活动性顺序和表中的信息,判断“镁与水蒸气”的反应情况为C、D
A.不反应 B.缓慢反应 C.比镁与冷水反应快 D.比铁与水蒸气反应快
(4)两位同学在讨论利用铁、铝的哪些物理性质来区分外形相同且厚度相同的铝做的锅和铁做的锅,请你想一想,写出两条:铝的密度小于铁的、铁能被磁体吸引;选择其中一条写出简要的实验步骤:用弹簧秤分别称铁锅和铝锅的重,较重的是铁锅,较轻的是铝锅(或
用以磁体分别吸引两只锅,能被吸引的是铁锅,不能被吸引的是铝锅).(注:不能破坏锅体本身)
(1)金属锰也是一种重金属,在我们人体或一些动物体内经常会检测到多种重金属离子的存在,进而危害我们的健康,这是为什么?金属离子可通过食物链在生物体内大量富集.
(2)某同学对金属锰、金属镁、金属铜的金属活泼性情况进行简单的实验如下,将金属锰分别放入硫酸镁和硫酸铜溶液中,分别记录现象如下:
| 硫酸镁 | 硫酸铜 | |
| 现象 | 无现象 | 有红色物质析出 |
(3)常见金属中有些能和水或水蒸汽发生反应,请根据金属活动性顺序和表中的已知信息回答:
| 物质 | 镁与冷水 | 镁与水蒸汽 | 铁与冷水 | 铁与水蒸气 | 铜与冷水 | 铜与水蒸气 |
| 反应情况 | 缓慢反应 | 不反应 | 能反应 | 不反应 | 不反应 |
A.不反应 B.缓慢反应 C.比镁与冷水反应快 D.比铁与水蒸气反应快
(4)两位同学在讨论利用铁、铝的哪些物理性质来区分外形相同且厚度相同的铝做的锅和铁做的锅,请你想一想,写出两条:铝的密度小于铁的、铁能被磁体吸引;选择其中一条写出简要的实验步骤:用弹簧秤分别称铁锅和铝锅的重,较重的是铁锅,较轻的是铝锅(或
用以磁体分别吸引两只锅,能被吸引的是铁锅,不能被吸引的是铝锅).(注:不能破坏锅体本身)
3.某实验小组欲证明氧化铜能加快氯酸钾的分解,他们进行了如下实验:
①称取mg胆矾晶体,研细后加入蒸馏水全部溶解;
②将足量的NaOH溶液与上述溶液充分反应,生成蓝色沉淀,过滤后洗涤沉淀;
③将所得沉淀转移到坩埚中,均匀缓慢加热至完全变为黑色,研细备用;
④按表中的质量混合好固体,在相同条件下加热,进行比较,其它可能影响实验的因素均忽略.
回答下列问题:
(1)请写出上述实验步骤③中涉及到的化学方程式:Cu(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CuO+H2O
(2)表格中的“待测数据”是指生成一定量气体所需时间.
(3)为使本实验具有说服力,在本实验中CuO的质量应取x=0.5g.
(4)如果要进一步探究CuO在反应中是否起到催化作用,请完成后续实验.(提示:可从催化剂的概念完成实验.)
①称取mg胆矾晶体,研细后加入蒸馏水全部溶解;
②将足量的NaOH溶液与上述溶液充分反应,生成蓝色沉淀,过滤后洗涤沉淀;
③将所得沉淀转移到坩埚中,均匀缓慢加热至完全变为黑色,研细备用;
④按表中的质量混合好固体,在相同条件下加热,进行比较,其它可能影响实验的因素均忽略.
| 编号 | KClO3质量(g) | 加入物质质量(g) | 待测数据 |
| 1 | 2.0 | CuO x | |
| 2 | 2.0 | MnO2 0.5 |
(1)请写出上述实验步骤③中涉及到的化学方程式:Cu(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CuO+H2O
(2)表格中的“待测数据”是指生成一定量气体所需时间.
(3)为使本实验具有说服力,在本实验中CuO的质量应取x=0.5g.
(4)如果要进一步探究CuO在反应中是否起到催化作用,请完成后续实验.(提示:可从催化剂的概念完成实验.)
| 实验步骤 | 设计这一步骤的目的 |
| 实验表明,加入CuO后产生O2的速率比未加入时快得多 | CuO能加快KClO3的分解 |
| 将加热后残留的固体溶于足量的水,过滤后称重CuO的质量 | CuO的质量在反应前后是否保持不变 |
| 将过滤后的CuO重新与KClO3混合加热,观察是否依旧能加快KClO3的分解(或者利用CuO的常见化学性质如:将CuO加入稀硫酸中,观察无色溶液是否变成蓝色) | CuO的化学性质在反应前后是否保持不变 |
20.向一定量的碳酸钠溶液中加入一定量的氢氧化钙溶液,充分反应后过滤.你认为滤液中溶质的组成最多有3种情况,这几种情况中一定都含有的溶质是(填写化学式)NaOH. 为了证明上述实验中碳酸钠和氢氧化钙溶液恰好完全反应,某同学设计以下实验,请将有关内容在下列横线上填写完整.
| 验证的实验方法 | 观察到的实验现象 | 结论 |
| (1)取样,加Na2CO3溶液 | 无现象 | 没有氢氧化钙 |
| (2)另取样,加稀盐酸溶液 | 无现象 | 证明两者刚好完全反应 |
19.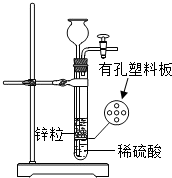 图为实验室制取氢气的发生装置.若液面刚好不与锌粒接触而又无酸液可加,要得到氢气且不影响氢气的制取量,可从长颈漏斗中加入适量试剂的一组是( )
图为实验室制取氢气的发生装置.若液面刚好不与锌粒接触而又无酸液可加,要得到氢气且不影响氢气的制取量,可从长颈漏斗中加入适量试剂的一组是( )
①食盐水 ②硫酸钠溶液 ③氯化钡溶液 ④碳酸钠溶液 ⑤氢氧化钠.
0 166662 166670 166676 166680 166686 166688 166692 166698 166700 166706 166712 166716 166718 166722 166728 166730 166736 166740 166742 166746 166748 166752 166754 166756 166757 166758 166760 166761 166762 166764 166766 166770 166772 166776 166778 166782 166788 166790 166796 166800 166802 166806 166812 166818 166820 166826 166830 166832 166838 166842 166848 166856 211419
 图为实验室制取氢气的发生装置.若液面刚好不与锌粒接触而又无酸液可加,要得到氢气且不影响氢气的制取量,可从长颈漏斗中加入适量试剂的一组是( )
图为实验室制取氢气的发生装置.若液面刚好不与锌粒接触而又无酸液可加,要得到氢气且不影响氢气的制取量,可从长颈漏斗中加入适量试剂的一组是( )①食盐水 ②硫酸钠溶液 ③氯化钡溶液 ④碳酸钠溶液 ⑤氢氧化钠.
| A. | ①②③ | B. | ①②④ | C. | ①②⑤ | D. | ②③④ |
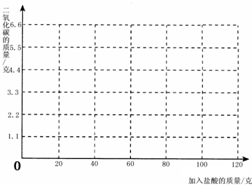 某白色固体混合物中含有氢氧化钠和碳酸钠这两种物质,取14.6g该混合物,向混合物中逐滴滴入10%的盐酸溶液,产生并收集到CO2气体(假设反应后CO2完全逸出)4.4g
某白色固体混合物中含有氢氧化钠和碳酸钠这两种物质,取14.6g该混合物,向混合物中逐滴滴入10%的盐酸溶液,产生并收集到CO2气体(假设反应后CO2完全逸出)4.4g