18.下列做法正确的是( )
| A. | 用过滤的方法降低水的硬度 | B. | 用金刚石裁割玻璃 | ||
| C. | 用甲醛溶液浸泡海产品 | D. | 用石灰石改良酸性土壤 |
17.现在有集气瓶盛装的四瓶无色无味的气体,已知他们分别是:氧气、氮气、二氧化碳和空气,请设计实验将他们鉴别开来(不考虑鉴别开以后,气体是否已经受到污染).
| 实验步骤 | 实验现象 | 实验结论 |
| 1.用带火星的木条分别伸入四个集气瓶中 | 其中一瓶气体能使带火星的木条复燃 | 能使带火星的木条复燃的那一瓶是氧气. |
| 2.往剩余的三个集气瓶中,分别倒入少量澄清石灰水,震荡. | 其中一瓶气体能使澄清的石灰水变浑浊 | 能使澄清石灰水变浑浊的那一瓶是二氧化碳 |
| 3.用燃着的木条伸入剩余的两个集气瓶中. | 其中一瓶气体能使火焰熄灭 | 能使火焰熄灭熄灭的是氮气 |
15.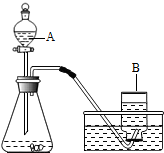 在实验室里,常用分解过氧化氢溶液、加热氯酸钾或高锰酸钾制取氧气.某化学兴趣小组对氧气的实验室制法进行了探究.
在实验室里,常用分解过氧化氢溶液、加热氯酸钾或高锰酸钾制取氧气.某化学兴趣小组对氧气的实验室制法进行了探究.
(1)小明同学选用如图所示的装置制取氧气.制取过程中所发生的化学反应方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.实验前,小明同学先向仪器A中加入水,然后将导气管放入水槽中,并打开仪器A的活塞,观察导气管口是否有连续的气泡出现.该实验操作的目的是检查装置的气密性.
(2)小红同学通过互联网得知:CuSO4 溶液、动物某些脏器中含有的物质等能催化过氧化氢的分解.动物脏器中含有过氧化氢酶,能催化过氧化氢分解,过氧化氢酶是蛋白质(选填糖类、蛋白质、脂肪或维生素),实验证明,CuSO4 溶液能催化过氧化氢的分解.CuSO4溶液主要含有三种粒子(H2O、Cu2+、SO42-),为了进一步探究CuSO4溶液中哪种粒子能起催化作用.小红同学作了如下分析和设计.
①小红同学认为最不可能的是H2O,他的理由是过氧化氢溶液中含有水.
②要说明另外的两种粒子是否起到催化作用,小红同学设计了如下实验,完成了这次探究活动.
③如果要确定CuSO4是催化剂,还必须通过实验确定它在化学反应前后质量和化学性质没有改变.
 在实验室里,常用分解过氧化氢溶液、加热氯酸钾或高锰酸钾制取氧气.某化学兴趣小组对氧气的实验室制法进行了探究.
在实验室里,常用分解过氧化氢溶液、加热氯酸钾或高锰酸钾制取氧气.某化学兴趣小组对氧气的实验室制法进行了探究.(1)小明同学选用如图所示的装置制取氧气.制取过程中所发生的化学反应方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.实验前,小明同学先向仪器A中加入水,然后将导气管放入水槽中,并打开仪器A的活塞,观察导气管口是否有连续的气泡出现.该实验操作的目的是检查装置的气密性.
(2)小红同学通过互联网得知:CuSO4 溶液、动物某些脏器中含有的物质等能催化过氧化氢的分解.动物脏器中含有过氧化氢酶,能催化过氧化氢分解,过氧化氢酶是蛋白质(选填糖类、蛋白质、脂肪或维生素),实验证明,CuSO4 溶液能催化过氧化氢的分解.CuSO4溶液主要含有三种粒子(H2O、Cu2+、SO42-),为了进一步探究CuSO4溶液中哪种粒子能起催化作用.小红同学作了如下分析和设计.
①小红同学认为最不可能的是H2O,他的理由是过氧化氢溶液中含有水.
②要说明另外的两种粒子是否起到催化作用,小红同学设计了如下实验,完成了这次探究活动.
| 实验步骤 | 实验现象 | 结论 |
| a.取一支试管加入5mL5%过氧化氢溶液,然后加入2~3滴稀硫酸溶液 | 溶液几乎没有气泡放出 | 实验证明,起催化作用的是Cu2+ |
| b.另取一支试管加入5mL5%过氧化氢溶液,然后加入2~3滴氯化铜溶液 | 溶液中有大量产泡放出 |
14. 某化学小组以“酸碱盐”为主题,进行了一系列的实验探究活动.
某化学小组以“酸碱盐”为主题,进行了一系列的实验探究活动.
探究1:研究常见的物质--氢氧化钠和盐酸的反应程度.
探究2:研究酸的性质--硫酸、盐酸和锌反应通过探究实验,同学们发现硫酸和盐酸溶液都可以和锌反应产生氢气.产生这种共同现象的原因为硫酸和盐酸溶液中都含有氢离子.
探究3:探索未知--浓硝酸和铜制取气体.
已知Cu+4HNO3(浓)═Cu(NO3)2+2H2O+2NO2↑.NO2能和水反应生成硝酸和NO.NO和NO2都是空气的污染物.
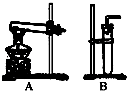
(1)利用该反应制取二氧化氮,其发生装置应选用右图所示装置中的.收集NO2的方法为向上排空气法.
(2)NO为无色气体,其和空气接触会变为红棕色,这是因为NO和空气中的氧气发生化合反应生成了NO2,其反应的化学方程式为:2NO+O2═2N02
探究4:兴趣小组同学向盛有澄清石灰水1000g的大烧杯中加入10g碳酸钠溶液,恰好完全反应后过滤去沉淀,剩余液体总质量为1009.8g,请你计算所加碳酸钠溶液的溶质质量分数?
 某化学小组以“酸碱盐”为主题,进行了一系列的实验探究活动.
某化学小组以“酸碱盐”为主题,进行了一系列的实验探究活动.探究1:研究常见的物质--氢氧化钠和盐酸的反应程度.
| 实验内容 | 实验现象 | 解释与结论 |
| 取反应后少量溶液于试管中,加入固体化合物. | (加CaCO3),有气泡产生. | 盐酸过量 |
探究3:探索未知--浓硝酸和铜制取气体.
已知Cu+4HNO3(浓)═Cu(NO3)2+2H2O+2NO2↑.NO2能和水反应生成硝酸和NO.NO和NO2都是空气的污染物.
(1)利用该反应制取二氧化氮,其发生装置应选用右图所示装置中的.收集NO2的方法为向上排空气法.
(2)NO为无色气体,其和空气接触会变为红棕色,这是因为NO和空气中的氧气发生化合反应生成了NO2,其反应的化学方程式为:2NO+O2═2N02
探究4:兴趣小组同学向盛有澄清石灰水1000g的大烧杯中加入10g碳酸钠溶液,恰好完全反应后过滤去沉淀,剩余液体总质量为1009.8g,请你计算所加碳酸钠溶液的溶质质量分数?
12.在一次化学实验操作考核中,某同学有如下操作和应急措施,其中不正确的是( )
| A. |  酒精灯失火用湿抹布扑盖 | B. |  将NaCl倒入量筒中配制溶液 | ||
| C. |  研磨闻气味鉴别铵态氮肥 | D. |  分离浑浊河水中的不溶物 |
11.下列生活物品中,用有机合成材料制作的是( )
0 166571 166579 166585 166589 166595 166597 166601 166607 166609 166615 166621 166625 166627 166631 166637 166639 166645 166649 166651 166655 166657 166661 166663 166665 166666 166667 166669 166670 166671 166673 166675 166679 166681 166685 166687 166691 166697 166699 166705 166709 166711 166715 166721 166727 166729 166735 166739 166741 166747 166751 166757 166765 211419
| A. | 铝合金门窗 | B. | 玻璃杯 | C. | 塑料洗衣盆 | D. | 陶瓷碗 |


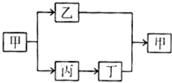 有甲、乙、丙三种常见的单质或化合物,有如图所示转化关系,其它试剂或条件任选,则甲为:CD.
有甲、乙、丙三种常见的单质或化合物,有如图所示转化关系,其它试剂或条件任选,则甲为:CD.