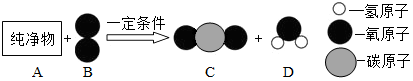
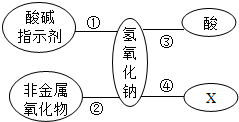
题目内容
14. 某化学小组以“酸碱盐”为主题,进行了一系列的实验探究活动.
某化学小组以“酸碱盐”为主题,进行了一系列的实验探究活动.探究1:研究常见的物质--氢氧化钠和盐酸的反应程度.
| 实验内容 | 实验现象 | 解释与结论 |
| 取反应后少量溶液于试管中,加入固体化合物. | (加CaCO3),有气泡产生. | 盐酸过量 |
探究3:探索未知--浓硝酸和铜制取气体.
已知Cu+4HNO3(浓)═Cu(NO3)2+2H2O+2NO2↑.NO2能和水反应生成硝酸和NO.NO和NO2都是空气的污染物.
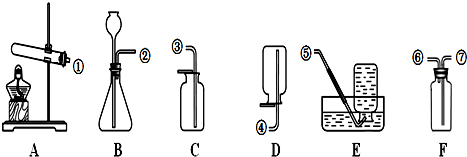
(1)利用该反应制取二氧化氮,其发生装置应选用右图所示装置中的.收集NO2的方法为向上排空气法.
(2)NO为无色气体,其和空气接触会变为红棕色,这是因为NO和空气中的氧气发生化合反应生成了NO2,其反应的化学方程式为:2NO+O2═2N02
探究4:兴趣小组同学向盛有澄清石灰水1000g的大烧杯中加入10g碳酸钠溶液,恰好完全反应后过滤去沉淀,剩余液体总质量为1009.8g,请你计算所加碳酸钠溶液的溶质质量分数?
分析 探究一:根据酸的化学性质分析;
探究二:根据酸的定义及特征分析;
探究三:根据反应物的状态和反应条件选择发生装置,根据溶解性和密度选择收集方法,根据质量守恒定律书写方程式.
探究四:根据化学方程式的计算分析.
解答 解:探究一:因盐酸能与碳酸盐反应产生气泡的明显现象,可以用来检验盐酸,故答案为:Na2CO3(或CaCO3),有气泡产生.
探究二:酸的共同特征是电离出的阳离子都是氢离子,决定了酸具有相似的化学性质.故答案为:硫酸和盐酸溶液中都含有氢离子.
探究三:(1)制取二氧化氮的反应物状态和反应条件属于固液、常温型,故选B;有因为二氧化氮易与水反应,故不能用排水法收集,根据相对分子质量法比较:46>29可知二氧化氮的密度大于空气,故采用向上排空气法收集.
(2)因为NO和空气中的氧气发生化合反应生成了NO2,根据质量守恒定律,其反应的化学方程式为:2NO+O2═2N02.
探究四:根据反应前后的质量差可知,生成CaCO3沉淀的质量为1000g+10g-1009.8g=0.2g
设:反应物中Na2CO3的质量为x
Na2CO3+Ca(OH)2═CaCO3↓+2NaOH
106 100
x 0.2g
$\frac{106}{100}$=$\frac{x}{0.2g}$
x=0.212g
碳酸钠溶液溶质质量分数为:0.212g/10g×100%=2.12%
答:所加碳酸钠溶液的溶质质量分数为2.12%.
答案为:故探究1:(加CaCO3),有气泡产生.
探究2:硫酸和盐酸溶液中都含有氢离子;
探究3:(1)向上排空气法; (2)2NO+O2═2N02;
探究4:2.12%.
点评 此题考查的内容较多,要逐一分析解答.

练习册系列答案
相关题目
19.规范实验操作是获得实验成功的重要保证.如图所示化学实验操作不正确的是( )
| A. | 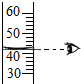 读出液体的体积 | B. | 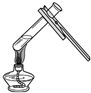 给液体加热 | C. | 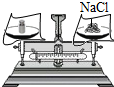 称取固体NaCl | D. | 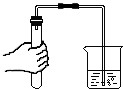 检查气密性 |
6.下列对物质的分类正确的是( )
| A. | 尿素、氨水、碳酸氢钠属于氮肥 | B. | 萘、铁、冰属于晶体 | ||
| C. | 干木头、金属、石墨属于导体 | D. | 酱油、黑芝麻糊、蒸馏水属于混合物 |
4.下列观点我不同意的是( )
| A. | 酸中肯定含有氢元素 | |
| B. | 碱一定由金属阳离子与氢氧根离子结合形成 | |
| C. | 分子的质量一定大于原子的质量 | |
| D. | 空气中含量最多的元素是氮 |