题目内容
15.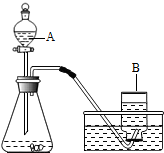 在实验室里,常用分解过氧化氢溶液、加热氯酸钾或高锰酸钾制取氧气.某化学兴趣小组对氧气的实验室制法进行了探究.
在实验室里,常用分解过氧化氢溶液、加热氯酸钾或高锰酸钾制取氧气.某化学兴趣小组对氧气的实验室制法进行了探究.(1)小明同学选用如图所示的装置制取氧气.制取过程中所发生的化学反应方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.实验前,小明同学先向仪器A中加入水,然后将导气管放入水槽中,并打开仪器A的活塞,观察导气管口是否有连续的气泡出现.该实验操作的目的是检查装置的气密性.
(2)小红同学通过互联网得知:CuSO4 溶液、动物某些脏器中含有的物质等能催化过氧化氢的分解.动物脏器中含有过氧化氢酶,能催化过氧化氢分解,过氧化氢酶是蛋白质(选填糖类、蛋白质、脂肪或维生素),实验证明,CuSO4 溶液能催化过氧化氢的分解.CuSO4溶液主要含有三种粒子(H2O、Cu2+、SO42-),为了进一步探究CuSO4溶液中哪种粒子能起催化作用.小红同学作了如下分析和设计.
①小红同学认为最不可能的是H2O,他的理由是过氧化氢溶液中含有水.
②要说明另外的两种粒子是否起到催化作用,小红同学设计了如下实验,完成了这次探究活动.
| 实验步骤 | 实验现象 | 结论 |
| a.取一支试管加入5mL5%过氧化氢溶液,然后加入2~3滴稀硫酸溶液 | 溶液几乎没有气泡放出 | 实验证明,起催化作用的是Cu2+ |
| b.另取一支试管加入5mL5%过氧化氢溶液,然后加入2~3滴氯化铜溶液 | 溶液中有大量产泡放出 |
分析 (1)从题目中装置的特点是固体和液体反应且不需要加热,故所选的药品为过氧化氢溶液和二氧化锰;加药品前一定要先检查装置的气密性去分析;
(2)从过氧化氢酶是蛋白质的一种;由于过氧化氢溶液中含有大量的水分去分析;
(3)a.从取一支试管加入5mL5%过氧化氢溶液,然后加入2~3滴稀硫酸溶液(硫酸溶液中含有氢离子和硫酸根离子),溶液几乎没有气泡放出,说明硫酸根离子对过氧化氢溶液不起催化作用;结合上面的结论可知是硫酸铜溶液中起到催化作用的应该是Cu2+,所以在步骤b中可加入氯化铜溶液(溶液中含有铜离子).
③从催化剂的特点是改变其他物质的反应速率,而本身的质量和化学性质不变去分析.
解答 解:(1)题目中装置的特点是固体和液体反应且不需要加热,故所选的药品为过氧化氢溶液和二氧化锰;过氧化氢溶液在二氧化锰催化作用下生成水和氧气,二氧化锰在反应前后质量和化学性质都没有改变,只是加快了过氧化氢反应生成氧气的速率,故二氧化锰是催化剂,所以二氧化锰就应该作为反应条件写在等号的上方,故化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,加药品前一定要先检查装置的气密性,防止加热过程中因装置漏气而收集不到制取的氧气,“实验前,小明同学先向仪器A中加入水,然后将导气管放入水槽中,并打开仪器A的活塞,观察导气管口是否有连续的气泡出现”如果有气泡冒出,说明装置的气密性好,否则装置漏气;故答案为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑ 检查装置的气密性;
(2)过氧化氢酶是蛋白质的一种;由于过氧化氢溶液中含有大量的水分,故可以得出水分子不可能起催化作用;故答案为:蛋白质 过氧化氢溶液中含有水;
(3)a.取一支试管加入5mL5%过氧化氢溶液,然后加入2~3滴稀硫酸溶液(硫酸溶液中含有氢离子和硫酸根离子),溶液几乎没有气泡放出,说明硫酸根离子对过氧化氢溶液不起催化作用;结合上面的结论可知是硫酸铜溶液中起到催化作用的应该是Cu2+,所以在步骤b中可加入氯化铜溶液(溶液中含有铜离子).可以故答案为:
| 实验步骤 | 实验现象 | 结论 |
| Cu2+ | ||
| 氯化铜 |
点评 本题主要考查了氧气的实验室制法的反应原理、注意事项、催化剂的有关实验等,综合性较强,是常考的知识点之一.

 名校课堂系列答案
名校课堂系列答案| A. | 用氯化钾制氯化钠KCl+NaNO3=NaCl+KNO3 | |
| B. | 用二氧化碳制碳酸饮料CO2+H2O=H2CO3 | |
| C. | 用电解水的方法测定水的组成2H2O=2H2↑+O2↑ | |
| D. | 用氢氧化钠制碳酸钠Na2CO3+Ca(OH)2=CaCO3↓+2NaOH |
| A. | 酚酞溶液、“雪碧”饮料 | B. | NaOH溶液、酚酞溶液 | ||
| C. | CuSO4溶液、NaOH溶液 | D. | 紫色石蕊溶液、酚酞溶液 |
| A. | 二氧化碳(一氧化碳)--通过足量的氢氧化钠溶液、干燥 | |
| B. | 硫酸亚铁溶液(硫酸铜)--加过量的锌粉、过滤 | |
| C. | 氢氧化钠(碳酸钠)--加适量的稀盐酸、蒸发 | |
| D. | 氮气(氧气)--通过灼热的铜网 |
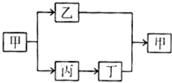 有甲、乙、丙三种常见的单质或化合物,有如图所示转化关系,其它试剂或条件任选,则甲为:CD.
有甲、乙、丙三种常见的单质或化合物,有如图所示转化关系,其它试剂或条件任选,则甲为:CD. 化学与生活、生产关系密切.请回答下列问题:
化学与生活、生产关系密切.请回答下列问题: