15.已知所含元素化合价发生变化的反应是氧化还原反应,其中被还原的元素化合价降低,被氧化的元素化合价升高.海洋中有丰富的资源,如图所示利用海水可获得许多化工产品.下列有关说法正确的是( )


| A. | 第①步中除去粗盐中的SO42-、Ca2+、Mg2+等杂质,加入的试剂顺序为:NaOH溶液、Na2CO3溶液、BaCl2溶液,过滤后加盐酸 | |
| B. | 第②步中加入的试剂为CaCl2溶液 | |
| C. | 第③步中发生氧化还原反应 | |
| D. | 在第④步中溴元素被还氧化 |
14.在已经调平的托盘天平两边各放一只等质量的烧杯,向烧杯中各加入质量相等.质量分数相等的稀硫酸,然后在左右两盘的烧杯中分别放入等质量的锌粉和铁粉.下列实验现象不可能观察到的是( )
| A. | 天平指针开始偏向放铁粉的烧杯一边 | |
| B. | 两只烧杯最终可能有一只烧杯有金属剩余 | |
| C. | 天平指针最终偏向放铁粉的烧杯一边 | |
| D. | 天平最终平衡 |
13.连二亚硫酸钠(Na2S2O4),也称保险粉,广泛用于纺织工业,属于一级遇湿易燃物品.下列有关连二亚硫酸钠的认识正确的是( )
| A. | 连二亚硫酸钠与水能剧烈反应,化学性质很活泼 | |
| B. | 连二亚硫酸钠是一种盐,硫元素化合价为+6价 | |
| C. | 连二亚硫酸钠俗称“保险粉”,原因是化学性质很稳定 | |
| D. | 连二亚硫酸钠俗称“保险粉”,无须密封保存 |
11.能证明“CaCO3并非绝对不溶于水”的实验事实是( )
| A. | 取0.5gCaCO3粉末于试管中,加入过量稀盐酸,充分振荡,粉末消失且有气泡产生 | |
| B. | 取0.5gCaCO3粉末于试管中,加入过量硫酸,充分振荡后,产生少许气泡,粉末未消失 | |
| C. | 取0.5gCaCO3粉末于试管中,加入3mL蒸馏水,充分振荡后,滴入酚酞试液,立即变红 | |
| D. | 取0.5gCaCO3粉末于试管中,加入3mL蒸馏水,充分振荡后,滴加10%NaOH溶液,无明显现象 |
10.已知:2NO+O2═2NO2,在一个密闭容器中,充入a个NO分子和b个O2分子,充分反应后,容器内氮原子个数和氧原子个数之比是( )
| A. | $\frac{a}{2b}$ | B. | $\frac{a}{2(a+b)}$ | C. | $\frac{a}{b}$ | D. | $\frac{a}{(a+2b)}$ |
9.甲、乙、丙、丁四个化学课外兴趣小组同学分别对各自实验废液中成分进行分析检测,结果如表;检测结果合理的是( )
0 166291 166299 166305 166309 166315 166317 166321 166327 166329 166335 166341 166345 166347 166351 166357 166359 166365 166369 166371 166375 166377 166381 166383 166385 166386 166387 166389 166390 166391 166393 166395 166399 166401 166405 166407 166411 166417 166419 166425 166429 166431 166435 166441 166447 166449 166455 166459 166461 166467 166471 166477 166485 211419
| 检测小组 | 检测结果 |
| 甲组 | KCl、FeCl3、KOH、HCl |
| 乙组 | NaCl、Ca(NO3)2、K2CO3、HCl |
| 丙组 | NaCl、Mg(NO3)2、K2SO4、H2SO4 |
| 丁组 | KCl、KNO3、K2CO3、KOH |
| A. | 甲组、乙组 | B. | 丙组、丁组 | C. | 甲组、丙组 | D. | 乙组、丁组 |
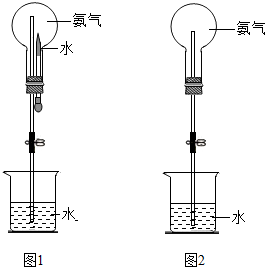 我国化学家侯德榜于1923年研制成功的“联合制碱法(又称侯氏制碱法)”的主要特点是:在浓氨水(NH3极易溶于水)中通入足量的二氧化碳生成一种盐,然后在此溶液中加入细的食盐粉末,由于NaHCO3在该状态下溶解度很小,呈晶体析出,同时由于大部分酸式碳酸盐加热容易转变为正盐,所以将析出的NaHCO3加热分解即可得纯碱,请回答:
我国化学家侯德榜于1923年研制成功的“联合制碱法(又称侯氏制碱法)”的主要特点是:在浓氨水(NH3极易溶于水)中通入足量的二氧化碳生成一种盐,然后在此溶液中加入细的食盐粉末,由于NaHCO3在该状态下溶解度很小,呈晶体析出,同时由于大部分酸式碳酸盐加热容易转变为正盐,所以将析出的NaHCO3加热分解即可得纯碱,请回答: