题目内容
17.在研究酸和碱的化学性质时,某化学兴趣小组的同学想证明:稀硫酸和氢氧化钠溶液混合后,虽然没有发生明显的变化,但确实发生了化学反应.请你与他们一起完成此实验的设计、实施和评价.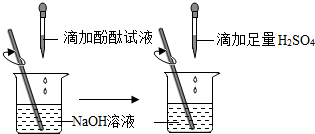
(1)方案一:测定稀硫酸和氢氧化钠溶液混合前后的pH(20℃).测定某NaOH溶液的pH,其pH大于7(选填“大于”、“小于”或“等于”).将一定量的稀硫酸加入该NaOH溶液中,混合均匀后测其pH,pH<7.
结论:稀硫酸和NaOH溶液发生了化学反应,并且稀硫酸过量.
(2)方案二:观察红色逐渐消失(根据图示实验步骤,概括方案要点)
结论:稀硫酸和NaOH溶液发生了化学反应.
(3)上述两个方案在设计上思想上的相同点是测定溶液反应前后的酸碱性变化来确定两种溶液混合后是否发生了化学反应.
(4)任何化学反应均伴随能量变化,中和反应均为放热反应.为了进一步获取稀硫酸与NaOH溶液确实发生了化学反应的证据,依据稀硫酸与NaOH溶液反应是放热(选填“放热”、“吸热”或“无热量变化”)的反应,采用同温下的稀硫酸与NaOH溶液进行实验,整个实验中至少需要测定溶液温度3次.
分析 (1)当溶液的pH等于7时,呈中性;当溶液的pH小于7时,呈酸性;当溶液的pH大于7时,呈碱性;据此根据氢氧化钠溶液的酸碱性进行分析判断.
根据题意,将一定量稀硫酸加入该氢氧化钠溶液中,混合均匀后测定混合溶液的pH小于7,则可判断出反应后酸过量.
(2)根据碱溶液遇酚酞溶液变红,利用酸碱反发生中和反应使碱减少,据此判断颜色的变化.
(3)方案一是测定溶液的pH来确定溶液酸碱性变化,方案二通过酸碱指示剂的颜色变化确定溶液的酸碱性变化,即都是测定溶液的酸碱性变化来判断反应是否发生.
(4)中和反应为放热反应,根据测定反应前后、过程中溶液的温度变化来确定至少测定的次数.
解答 解:(1)氢氧化钠溶液显碱性,其pH大于7;
(2)将一定量稀硫酸加入该氢氧化钠溶液中,混合均匀后测定混合溶液的pH小于7,说明稀硫酸与氢氧化钠溶液发生了化学反应,且稀硫酸过量.
酚酞溶液滴入到氢氧化钠溶液中显红色,当向氢氧化钠溶液中加入稀硫酸时,发生中和反应反应使碱减少至消失,则红色逐渐变浅直至消失.
(3)无论是测溶液的PH,还是酚酞颜色的变化,都与溶液的酸碱性变化有关.利用pH值,总结上述两个方案在设计思想上的相同点是 测定溶液反应前后的酸碱性变化来确定两种溶液混合后是否发生了化学反应.
(4)中和反应为放热反应,可以通过测定反应前后溶液的温度变化来进行确定,反应前测定起始温度,反应中测定温度是否升高,加入过量的硫酸再测定溶液的温度是否降低,故最少需要测定3次.
故答案为:(1)大于;H2SO4;(2)红色逐渐消失;(3)测定溶液反应前后的酸碱性变化来确定两种溶液混合后是否发生了化学反应;(4)放热;3.
点评 本题有一定难度,考查了中和反应及其应用,掌握中和反应、常见酸碱指示剂的性质、溶液的酸碱性和溶液pH大小之间的关系是正确解题的关键.

 阅读快车系列答案
阅读快车系列答案| A. | 煤气泄漏,应立即关闭阀门并开窗通风 | |
| B. | 为减少“白色污染”,可将塑料垃圾集中焚烧处理 | |
| C. | 木材着火,用水扑灭,是因为降低了木材的着火点 | |
| D. | 启用闲置的沼气池前,先用燃着的蜡烛进行灯火实验 |
| 物质(括号内为杂质) | 除杂所用试剂和方法 | |
| A | CO2(CO) | 点火燃烧 |
| B | Cu(Zn) | 加入足量稀硫酸,充分反应后过滤 |
| C | NaOH(Na2CO3) | 加入适量稀盐酸,充分反应后蒸发 |
| D | NaCl(Na2SO4) | 加入适量氯化钡溶液,充分反应后过滤、蒸发 |
| A. | A | B. | B | C. | C | D. | D |
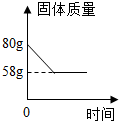 化学小组同学取一定量碳酸钙固体高温煅烧一段时间,冷却后,对剩余固体成分进行如下探究.
化学小组同学取一定量碳酸钙固体高温煅烧一段时间,冷却后,对剩余固体成分进行如下探究.【查阅资料】工业上通常采用高温煅烧石灰石的方法制生石灰,化学方程式为:
CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑.
该化学小组取80g的固体样品煅烧(杂质质量无变化),煅烧过程中固体质量变化如图所示,求:①碳酸钙中钙元素的质量分数为40%;
②该石灰石样品中碳酸钙的纯度.
【提出问题】煅烧后剩余固体成分是什么?
【猜想与假设】剩余固体成分:
I.全部是氧化钙Ⅱ.氧化钙和碳酸钙Ⅲ.全部是碳酸钙
在老师指导下,小组同学设计如下实验,探究上述猜想是否成立.
【进行实验】
①甲同学取一定量的剩余固体于试管中,加入一定量的水振荡,有白色不溶物.甲同学据此认为试管中的固体为碳酸钙,即猜想Ⅲ成立.乙同学认为上述实验不足以证明猜想Ⅲ成立,其理由是氧化钙与水反应生成的氢氧化钙微溶于水,也可能出现白色不溶物.
②乙同学取一定量的剩余固体于试管中,加入一定量的水,触摸试管外壁感觉发热,继续向试管中加入几滴稀盐酸,没有气泡产生.乙同学据此认为试管中的固体只有氧化钙,即猜想I成立.丙同学认为乙的实验不足以证明猜想I成立,理由是即使有碳酸钙,加入的少量稀盐酸先消耗氢氧化钙,也不会出现气泡.
③丙同学利用水、无色酚酞溶液和稀盐酸证明了猜想Ⅱ成立,请完成实验报告.
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量剩余固体于试管中,加水 振荡,过滤 取滤液滴加无色酚酞溶液 取滤渣滴加足量的稀盐酸 | 溶液变红 有气泡产生 | 猜想Ⅱ成立 |
A.气体肥料 B.制干冰 C.制纯碱 D.制碳酸饮料.