5.下列实验操作正确的是( )
| A. | 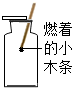 检验CO2是否集满 | B. | 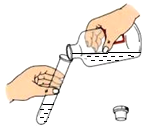 取用液体 | ||
| C. | 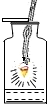 铁丝在氧气中燃烧 | D. | 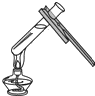 加热液体 |
4.以下日常生活中的做法科学的是( )
| A. | 往着火的油锅泼冷水 | B. | 把电吹风机放在潮湿的屋内 | ||
| C. | 经常擦磨铝制品以保持光亮 | D. | 将垃圾分类并回收处理 |
3. 如下猜想:可能部分变质,固体是NaOH和 Na2CO3的混合物;可能全部变质,固体是Na2CO3.
如下猜想:可能部分变质,固体是NaOH和 Na2CO3的混合物;可能全部变质,固体是Na2CO3.
(1)首先对固体的成分进行确定.取少量固体于试管中,加水充分溶解,先加入足量的BaCl2 溶液,产生白色沉淀,静置后取上层清液,再加入CuSO4 溶液,产生蓝色絮状沉淀.根据实验现象,可确定该固体是NaOH和Na2CO3 的混合物;
(2)称取10.6g 该固体样品于锥形瓶中,加入一定质量分数的稀盐酸,直至过量,得到数据如表:
计算该样品中Na2CO3的质量分数.
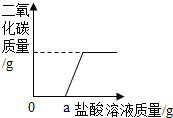
(3)再取固体样品溶于水,加入一定质量分数的稀盐酸,直至过量.测出加入稀盐酸的质量与产生CO2气体的质量关系如图所示.从图中可以判断:在该样品溶液中加入稀盐酸,首先与之反应的物质是NaOH.
(4)请你分析,一定质量的NaOH固体,变质前后与相同质量分数的稀盐酸反应,变质前消耗盐酸的量等于变质后消耗盐酸的量(填“大于”、“小于”或“等于”).
 如下猜想:可能部分变质,固体是NaOH和 Na2CO3的混合物;可能全部变质,固体是Na2CO3.
如下猜想:可能部分变质,固体是NaOH和 Na2CO3的混合物;可能全部变质,固体是Na2CO3.(1)首先对固体的成分进行确定.取少量固体于试管中,加水充分溶解,先加入足量的BaCl2 溶液,产生白色沉淀,静置后取上层清液,再加入CuSO4 溶液,产生蓝色絮状沉淀.根据实验现象,可确定该固体是NaOH和Na2CO3 的混合物;
(2)称取10.6g 该固体样品于锥形瓶中,加入一定质量分数的稀盐酸,直至过量,得到数据如表:
| 样品质量 | 反应前总质量 | 反应后总质量 |
| 10.6克 | 148.5克 | 146.3克 |
(3)再取固体样品溶于水,加入一定质量分数的稀盐酸,直至过量.测出加入稀盐酸的质量与产生CO2气体的质量关系如图所示.从图中可以判断:在该样品溶液中加入稀盐酸,首先与之反应的物质是NaOH.
(4)请你分析,一定质量的NaOH固体,变质前后与相同质量分数的稀盐酸反应,变质前消耗盐酸的量等于变质后消耗盐酸的量(填“大于”、“小于”或“等于”).
18. 有一包白色固体,可能含有BaCl2、KCl、K2SO4、K2CO3中的一种或几种.取样溶于水,有白色沉淀产生;过滤后向沉淀中滴加稀盐酸,沉淀的量与加入盐酸体积的关系如图所示.由此推断白色固体中( )
有一包白色固体,可能含有BaCl2、KCl、K2SO4、K2CO3中的一种或几种.取样溶于水,有白色沉淀产生;过滤后向沉淀中滴加稀盐酸,沉淀的量与加入盐酸体积的关系如图所示.由此推断白色固体中( )
 有一包白色固体,可能含有BaCl2、KCl、K2SO4、K2CO3中的一种或几种.取样溶于水,有白色沉淀产生;过滤后向沉淀中滴加稀盐酸,沉淀的量与加入盐酸体积的关系如图所示.由此推断白色固体中( )
有一包白色固体,可能含有BaCl2、KCl、K2SO4、K2CO3中的一种或几种.取样溶于水,有白色沉淀产生;过滤后向沉淀中滴加稀盐酸,沉淀的量与加入盐酸体积的关系如图所示.由此推断白色固体中( )| A. | 肯定只存在BaCl2 | B. | 可能存在K2SO4 | C. | 可能存在KCl | D. | 肯定不存在K2CO3 |
17.化学实验课时,同学们正在做比较金属活动性的实验,当他们将镁条放入某FeCl3溶液中时,意外发现镁条表面有气泡产生.对于这一异常现象产生的原因,同学们设计了探究方案进行讨论.其中没有意义的是( )
| A. | 甲同学推测气体可能是H2,并收集气体用点燃法检验 | |
| B. | 乙同学继续用镁条与该FeCl3溶液反应,观察产生气泡的快慢 | |
| C. | 丙同学用锌粒与该FeCl3溶液反应,观察是否有气泡产生 | |
| D. | 丁同学猜想该FeCl3溶液呈酸性,并用pH试纸检测 |
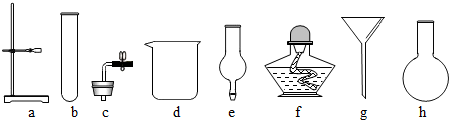
16.在没有现成的CO2气体发生器的情况下,请你选用如图中的部分仪器,装配成一个简易的、能随用随停的CO2气体发生器,应选用的仪器是( )
0 166159 166167 166173 166177 166183 166185 166189 166195 166197 166203 166209 166213 166215 166219 166225 166227 166233 166237 166239 166243 166245 166249 166251 166253 166254 166255 166257 166258 166259 166261 166263 166267 166269 166273 166275 166279 166285 166287 166293 166297 166299 166303 166309 166315 166317 166323 166327 166329 166335 166339 166345 166353 211419

| A. | a b c d | B. | a b d f | C. | a c d e | D. | a b c e |
 红枣包装中常使用一种袋装防腐剂,品名为“504 双 吸剂”,其标签如图所示. 同学们对一包久置的“504 双吸剂”固样品 很好奇,设计实验进行探究.
红枣包装中常使用一种袋装防腐剂,品名为“504 双 吸剂”,其标签如图所示. 同学们对一包久置的“504 双吸剂”固样品 很好奇,设计实验进行探究. 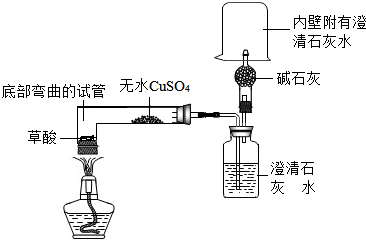 菠菜柔软滑嫩、味美色鲜,但菠菜中草酸含量较高,如果食用含草酸较多的食物,尿中草酸含量明显增多,尿路结石的危险性也随之增加.小科通过查资料得知,草酸的化学式为H2C2O4,并且草酸受热会分解,他对草酸受热分解及其产物的检验做了探究:
菠菜柔软滑嫩、味美色鲜,但菠菜中草酸含量较高,如果食用含草酸较多的食物,尿中草酸含量明显增多,尿路结石的危险性也随之增加.小科通过查资料得知,草酸的化学式为H2C2O4,并且草酸受热会分解,他对草酸受热分解及其产物的检验做了探究: