15.为探究气体X的组成,某兴趣小组进行如图所示实验(固定装置未画出).
【资料在线】
①加热条件下,气体X能与氧化铜反应生成铜、水和氮气.
②碱石灰为固体氢氧化钠和氧化钙的混合物,不与气体X反应.无水氯化钙可吸收气体X.
③本实验条件下,氮气密度为1.15g•L-1,装置内空气中的水与二氧化碳对相关数据测定的影响可忽略不计.
【实验步骤】
①连接仪器,并检查装置气密性.
②取一定量氧化铜,准确称得其质量为2.40g.
③按图所示装入药品(其中B、C管中分别装入的是足量碱石灰和足量无水氯化钙),测量并记录相关数据I(见表).
④连接A、B、C装置,将气体X缓缓通入一段时间后,连接上D装置,读数后开始加热.当A装置中氧化铜反应完全,停止加热,继续通入气体X至玻璃管冷却,再次测量并记录相关数据Ⅱ(见表).
【实验装置】
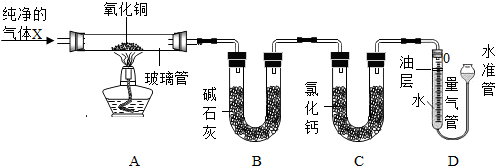
【相关数据】
【回答问题】
①B装置中氧化钙吸水的原理为CaO+H2O=Ca(OH)2(用化学方程式表示).
②实验过程中,当观察到量气管内液面不再下降,说明氧化铜已反应完全,停止加热,继续通入气体X至玻璃管冷却的目的是防止灼热的铜被氧化.
③分析实验测量的数据,生成水的质量为0.54g,氧化铜中氧元素的质量为0.48g.由此推知,气体X中一定没有(填“有”或“没有”)氧元素.
④通过计算推导出气体X的化学式为NH3;气体X还原氧化铜的化学方程式为:2NH3+3CuO$\frac{\underline{\;\;△\;\;}}{\;}$3Cu+3H2O+N2.
【资料在线】
①加热条件下,气体X能与氧化铜反应生成铜、水和氮气.
②碱石灰为固体氢氧化钠和氧化钙的混合物,不与气体X反应.无水氯化钙可吸收气体X.
③本实验条件下,氮气密度为1.15g•L-1,装置内空气中的水与二氧化碳对相关数据测定的影响可忽略不计.
【实验步骤】
①连接仪器,并检查装置气密性.
②取一定量氧化铜,准确称得其质量为2.40g.
③按图所示装入药品(其中B、C管中分别装入的是足量碱石灰和足量无水氯化钙),测量并记录相关数据I(见表).
④连接A、B、C装置,将气体X缓缓通入一段时间后,连接上D装置,读数后开始加热.当A装置中氧化铜反应完全,停止加热,继续通入气体X至玻璃管冷却,再次测量并记录相关数据Ⅱ(见表).
【实验装置】

【相关数据】
| 数据编号 测量项目 | I | Ⅱ |
| 玻璃管(含药品)的质量/g | 52.40 | 51.92 |
| B装置(含药品)的质量/g | 102.00 | 102.54 |
| 氮气的体积/mL | 243.5 |
①B装置中氧化钙吸水的原理为CaO+H2O=Ca(OH)2(用化学方程式表示).
②实验过程中,当观察到量气管内液面不再下降,说明氧化铜已反应完全,停止加热,继续通入气体X至玻璃管冷却的目的是防止灼热的铜被氧化.
③分析实验测量的数据,生成水的质量为0.54g,氧化铜中氧元素的质量为0.48g.由此推知,气体X中一定没有(填“有”或“没有”)氧元素.
④通过计算推导出气体X的化学式为NH3;气体X还原氧化铜的化学方程式为:2NH3+3CuO$\frac{\underline{\;\;△\;\;}}{\;}$3Cu+3H2O+N2.
13.人们在工作、生活中,为了防止事故,常采用一些安全措施,下列措施安全的是( )
| A. | 发生煤气泄漏,立即关闭阀门,打开门窗通风 | |
| B. | 掏空沼气池前进行灯火实验 | |
| C. | 点燃木条检查液化石油气是否泄漏 | |
| D. | 到小煤窑里挖煤用火把照明 |
11.填写下列表格:
| (1) | (2) | |||||
| 化学符号 | H | 2P2O5 | Al3+ | NH3 | ||
| 名称或意义(只写一种) | 2个金原子 | 由3个氧原子构成的一个臭氧分子 | ||||
10.在化学王国里,数字被赋予了丰富的内涵.对下列化学用语中数字“2”的说法正确的是( )
①2H ②2NH3③SO2④Mg2+⑤2OH-⑥H2O.
①2H ②2NH3③SO2④Mg2+⑤2OH-⑥H2O.
| A. | 表示离子个数的是④⑤ | B. | 表示分子中原子个数的是③⑥ | ||
| C. | 表示离子所带电荷数的是①⑤ | D. | 表示分子个数的是①② |
9.下列说法正确的是( )
| A. | 氨气是由一个氮原子和三个氢原子构成的 | |
| B. | 氨气是由氮气和氢气混合而成的 | |
| C. | 氨气是由氮、氢两种元素组成的 | |
| D. | 一个氨气分子是由一个氮元素和三个氢元素组成的 |
8.用量筒量取液体时,某同学先仰视凹液面的最低处,读数为19mL,倾倒一部分液体,又俯视凹液面最低处,读数为13mL,则这位同学取出的液体体积是( )
| A. | 等于6mL | B. | 小于6mL | C. | 大于6mL | D. | 无法判断 |
7.下列物质的用途,主要利用其化学性质的是( )
0 166009 166017 166023 166027 166033 166035 166039 166045 166047 166053 166059 166063 166065 166069 166075 166077 166083 166087 166089 166093 166095 166099 166101 166103 166104 166105 166107 166108 166109 166111 166113 166117 166119 166123 166125 166129 166135 166137 166143 166147 166149 166153 166159 166165 166167 166173 166177 166179 166185 166189 166195 166203 211419
| A. | 金刚石用来切割玻璃 | B. | 用氢气作探究空气球中的气体 | ||
| C. | 乙醇被用作内燃机中的燃料 | D. | 铝用于制造导线 |

 如图是电解水的装置,
如图是电解水的装置,