题目内容
15.为探究气体X的组成,某兴趣小组进行如图所示实验(固定装置未画出).【资料在线】
①加热条件下,气体X能与氧化铜反应生成铜、水和氮气.
②碱石灰为固体氢氧化钠和氧化钙的混合物,不与气体X反应.无水氯化钙可吸收气体X.
③本实验条件下,氮气密度为1.15g•L-1,装置内空气中的水与二氧化碳对相关数据测定的影响可忽略不计.
【实验步骤】
①连接仪器,并检查装置气密性.
②取一定量氧化铜,准确称得其质量为2.40g.
③按图所示装入药品(其中B、C管中分别装入的是足量碱石灰和足量无水氯化钙),测量并记录相关数据I(见表).
④连接A、B、C装置,将气体X缓缓通入一段时间后,连接上D装置,读数后开始加热.当A装置中氧化铜反应完全,停止加热,继续通入气体X至玻璃管冷却,再次测量并记录相关数据Ⅱ(见表).
【实验装置】
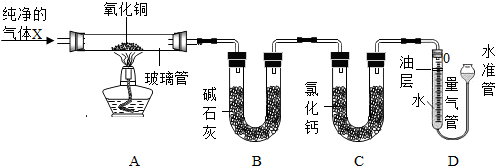
【相关数据】
| 数据编号 测量项目 | I | Ⅱ |
| 玻璃管(含药品)的质量/g | 52.40 | 51.92 |
| B装置(含药品)的质量/g | 102.00 | 102.54 |
| 氮气的体积/mL | 243.5 |
①B装置中氧化钙吸水的原理为CaO+H2O=Ca(OH)2(用化学方程式表示).
②实验过程中,当观察到量气管内液面不再下降,说明氧化铜已反应完全,停止加热,继续通入气体X至玻璃管冷却的目的是防止灼热的铜被氧化.
③分析实验测量的数据,生成水的质量为0.54g,氧化铜中氧元素的质量为0.48g.由此推知,气体X中一定没有(填“有”或“没有”)氧元素.
④通过计算推导出气体X的化学式为NH3;气体X还原氧化铜的化学方程式为:2NH3+3CuO$\frac{\underline{\;\;△\;\;}}{\;}$3Cu+3H2O+N2.
分析 根据题目的信息可知:B装置中的碱石灰为固体氢氧化钠和氧化钙的混合物,不与气体X反应,因此只吸收水蒸气,增加的质量就是生成的水的质量:102.54g-102.00g=0.54g;氧化铜中氧元素的质量=52.40g-51.92g=0.48g;由此推知,气体X中一定没有氧元素,因为0.54g水中氧元素的质量=0.54g×$\frac{16}{18}$=0.48g;B装置中氧化钙吸水的原理为:氧化钙和水反应生成氢氧化钙;实验过程中,当观察到量气管内液面不再下降,说明氧化铜已反应完全,停止加热,继续通入气体X至玻璃冷却的目的是防止灼热的铜被氧化;根据元素的质量比求x的化学式,有关的计算要准确.
解答 解:(1)B装置中氧化钙吸水的原理为:氧化钙和水反应生成氢氧化钙,化学方程式为:CaO+H2O=Ca(OH)2;
(2)实验过程中,当观察到量气管内液面不再下降,说明氧化铜已反应完全,停止加热,继续通入气体X至玻璃冷却的目的是防止灼热的铜被氧化;
(3)B装置中的碱石灰为固体氢氧化钠和氧化钙的混合物,不与气体X反应,因此只吸收水蒸气,增加的质量就是生成的水的质量:102.54g-102.00g=0.54g,0.54g水中氧元素的质量=0.54g×$\frac{16}{18}$=0.48g,氧化铜中氧元素的质量=52.40g-51.92g=0.48g,由此推知,气体X中一定没有氧元素;(4)243.5mL=0.2345L,设气体x的化学式为NmHn
$\frac{氮元素的质量}{氢元素的质量}$=$\frac{14m}{n}$=$\frac{1.15g/L×0.2435L}{0.54g-0.48g}$
$\frac{m}{n}$=$\frac{1}{3}$所以x的化学式为:NH3,氨气和氧化铜在加热的条件下生成铜、水和氮气:.
故答案为:NH3
故答案为:(1)CaO+H2O=Ca(OH)2;
(2)量气管内液面不再下降,防止灼热的铜被氧化;
(3)0.54,0.48,没有;
(4)2NH3+3CuO$\frac{\underline{\;\;△\;\;}}{\;}$3Cu+3H2O+N2.
点评 考点既考查了实验步骤的设计,又考查了化学方程式的书写和有关的计算等,还对实验进行了评价,综合性比较强,有关的计算要正确.同学们要具体分析,综合掌握.

| A. | 铁丝在氧气中燃烧时火星四射,有黑色四氧化三铁固体生成 | |
| B. | 铁钉与稀盐酸反应后溶液由无色变成了蓝色 | |
| C. | 硫在空气中燃烧发出微弱的淡蓝色火焰 | |
| D. | 红磷在空气中燃烧,冒大量的白雾 |
①2H ②2NH3③SO2④Mg2+⑤2OH-⑥H2O.
| A. | 表示离子个数的是④⑤ | B. | 表示分子中原子个数的是③⑥ | ||
| C. | 表示离子所带电荷数的是①⑤ | D. | 表示分子个数的是①② |
| A. | pH值越大,溶液的酸性越强;pH值越小,溶液的碱性越强 | |
| B. | CO2能与水反应生成碳酸,因此CO2溶于雨水会形成酸雨 | |
| C. | pH试纸既能测定溶液的酸碱性,又能测定溶液的酸碱度 | |
| D. | 测定溶液的pH值前,要先将pH试纸用蒸馏水润湿 |
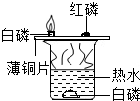 某同学为探究燃烧的条件,做了如图所示的实验.结果发现只有铜片上的白磷能燃烧,铜片上的红磷不能燃烧的原因是温度达不到着火点,热水中的白磷也不能燃烧的原因是没与氧气接触.请你对实验加以改进,使热水中的白磷燃烧起来用导管向烧杯中的白磷通入氧气(或空气).根据燃烧的条件写出下表灭火的原理:
某同学为探究燃烧的条件,做了如图所示的实验.结果发现只有铜片上的白磷能燃烧,铜片上的红磷不能燃烧的原因是温度达不到着火点,热水中的白磷也不能燃烧的原因是没与氧气接触.请你对实验加以改进,使热水中的白磷燃烧起来用导管向烧杯中的白磷通入氧气(或空气).根据燃烧的条件写出下表灭火的原理: 熄灭酒精灯火焰 |  房屋失火高压水枪喷水灭火 房屋失火高压水枪喷水灭火 |  防止火势蔓延,将部分树木砍掉 防止火势蔓延,将部分树木砍掉 |
| A. | 用磷测定空气中氧气的含量 4P+502=2P205氧化反应 | |
| B. | 用过氯化氢溶液制氧气 2H202$\frac{\underline{\;MnO_2\;}}{\;}$2H20+02↑ 化合反应 | |
| C. | 比较铜和银的活动性 Cu+2AgN03=Cu(N03)2+2Ag 置换反应 | |
| D. | 铁丝放入稀盐酸中 2Fe+6HCl=2FeCl3+3H2↑ 置换反应 |