题目内容
14.实验室给你提供了下列仪器,请选用合适的仪器完成指定的实验.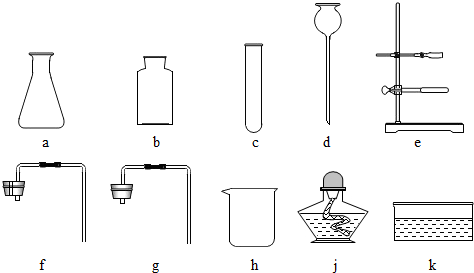
①图中仪器d的名称是:长颈漏斗.
②要制取较多的O2用来探究其性质(要求制取过程中可以添加反应物),组装气体发生装置需要的仪器是adf(填序号,下同),请写出该反应的化学方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,收集氧气应采用向上排空气法,这种收集方法是根据氧气的密度比空气的密度大性质.
③提纯粗盐时,过滤需要选用上述仪器中的eh(填序号),除此之外还缺少的仪器是滤纸、玻璃棒、漏斗(填名称).
分析 长颈漏斗方便加液体药品,制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.过滤用到的仪器有:烧杯、漏斗、玻璃棒、铁架台.
解答 解:(1)①长颈漏斗方便加液体药品;
(2)如果用双氧水和二氧化锰制氧气就不需要加热,要求制取过程中可以添加反应物,因此组装气体发生装置需要的仪器是:adf;过氧化氢在二氧化锰做催化剂的条件下生成水和氧气,要注意配平;氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集;
(3)过滤用到的仪器有:烧杯、漏斗、玻璃棒、铁架台;
故答案为:
(1)长颈漏斗;(2)adf;2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;向上排空气法;密度比空气的密度大;(3)eh;漏斗、玻璃棒.
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写、过滤操作,本考点是中考的重要考点之一,主要出现在实验题中.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
9.下列说法正确的是( )
| A. | 氨气是由一个氮原子和三个氢原子构成的 | |
| B. | 氨气是由氮气和氢气混合而成的 | |
| C. | 氨气是由氮、氢两种元素组成的 | |
| D. | 一个氨气分子是由一个氮元素和三个氢元素组成的 |
19.近年来,解决环境问题已成为人类面临的重要挑战之一.下列气体不会对环境造成影响的是( )
| A. | NO2 | B. | SO2 | C. | CO | D. | N2 |
3.水和溶液在生命活动和生活中起着十分重要的作用.
(1)海水中含有大量的氯化钠,可以通过日晒方法获得粗盐,粗盐提纯得到精盐.
(2)0.9%的氯化钠溶液称作生理盐水,其溶质是氯化钠.若用10%的NaCl溶液来配制
100g 0.9%的氯化钠溶液,需加水91g.
(3)熟石灰在部分温度下的溶解度如下表所示.
①20℃时,0.74g熟石灰放入到盛有100g水的烧杯中,搅拌,所得溶液中氢氧化钙的质
量减小(填“增大”、“减小”或“不变”),溶液中溶质的质量分数是0.2%.(精确到0.1%)
(1)海水中含有大量的氯化钠,可以通过日晒方法获得粗盐,粗盐提纯得到精盐.
(2)0.9%的氯化钠溶液称作生理盐水,其溶质是氯化钠.若用10%的NaCl溶液来配制
100g 0.9%的氯化钠溶液,需加水91g.
(3)熟石灰在部分温度下的溶解度如下表所示.
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 溶解度/g | 0.18 | 0.17 | 0.16 | 0.15 | 0.14 | 0.13 | 0.12 |
量减小(填“增大”、“减小”或“不变”),溶液中溶质的质量分数是0.2%.(精确到0.1%)
4.某化学反应的微粒变化如图所示,下列有关判断正确的是( )


| A. | 反应物的化学计量数之比为1:1 | B. | 生成物中一定不含氧化物 | ||
| C. | 反应前后原子、分子数目没有变化 | D. | 反应类型为化合反应 |