15.复习时,常用专题探究的方法学习常见物质的组成、性质与制取,课堂上老师引导我们回顾了几个探究实验.
探究1:研究常见物质组成

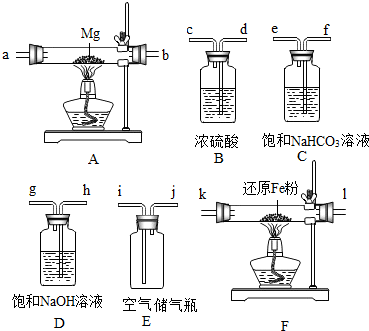
A、B、C都是研究物质组成的实验.从研究方法得知,A实验是利用可燃物消耗瓶内的氧气,使瓶内压强减小来推测空气里氧气含量的.B实验是通过证明生成物的元素组成来推断水的组成的.而C实验与B(填实验代号)实验的方法相同.
探究2:研究常见物质性质--氢氧化钠与硫酸是否刚好完全中和
(1)探索:用玻璃棒蘸取反应后的溶液滴在pH试纸上,发现该溶液的pH<7,说明硫酸过量.
(2)验证:
探究3:研究常见物质制取--制取氢氧化钠溶液
小京同学向盛有澄清石灰水的烧杯中加入过量的碳酸钠溶液,生成白色沉淀,过滤后得到无色溶液,他说:“我制得了氢氧化钠溶液!”
小欢同学却说:“这种无色溶液中不一定含有氢氧化钠.”他提出了如下实验:
小妮认为小欢的实验方案也不严密,不能证实无色溶液中一定含有氢氧化钠,理由是碳酸钠溶液也能使酚酞试液变红色.
小妮设计了另一个实验:
我认为:小欢和小妮的实验是为了证实小京结论的可靠性,小京的结论不可靠,原因
是氢氧化钠溶液中含有碳酸钠.显然小妮的实验可靠性比小欢的实验好,原因是排除了碳酸钠溶液的干扰.
探究1:研究常见物质组成

A、B、C都是研究物质组成的实验.从研究方法得知,A实验是利用可燃物消耗瓶内的氧气,使瓶内压强减小来推测空气里氧气含量的.B实验是通过证明生成物的元素组成来推断水的组成的.而C实验与B(填实验代号)实验的方法相同.
探究2:研究常见物质性质--氢氧化钠与硫酸是否刚好完全中和
(1)探索:用玻璃棒蘸取反应后的溶液滴在pH试纸上,发现该溶液的pH<7,说明硫酸过量.
(2)验证:
| 实验内容 | 实验现象 | 解释与结论 |
| 取反应后少量溶液于试管中,加入 碳酸钠溶液 | 产生气泡 | 证明研究结论正确 |
小京同学向盛有澄清石灰水的烧杯中加入过量的碳酸钠溶液,生成白色沉淀,过滤后得到无色溶液,他说:“我制得了氢氧化钠溶液!”
小欢同学却说:“这种无色溶液中不一定含有氢氧化钠.”他提出了如下实验:
| 实验步骤 | 实验现象 | 实验结论 |
| 用试管取无色溶液少许,滴入2滴无色酚酞试液 | 无色酚酞试液变红 | 无色溶液中含有氢氧化钠 |
小妮设计了另一个实验:
| 实验步骤 | 实验现象 | 实验结论 |
用试管取无色溶液少许,加入过量的氯化钙溶液,再滴加适量的酚酞试液 | 酚酞试液变红色 | 无色溶液中确实 含有氢氧化钠 |
是氢氧化钠溶液中含有碳酸钠.显然小妮的实验可靠性比小欢的实验好,原因是排除了碳酸钠溶液的干扰.
12.在一密闭容器中放入X、Y、Z、W四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表.则关于此反应的认识不正确的是( )
| 物质 | X | Y | Z | W |
| 反应前的质量(g) | 2 | 1 | 16 | 16 |
| 反应后的质量(g) | 17 | m | 6 | 11 |
| A. | 该反应的化学方程式为:3X+Y=2Z+W | B. | 该反应的基本类型为化合反应 | ||
| C. | Y在反应中可能起催化作用 | D. | 反应后容器中Z与Y的质量比为6:1 |
11.向氧化铜和铁粉的混合物中加入一定量的盐酸,微微加热,直至不再发生反应时反应容器中仍有少量固体物质存在,这少量固体物质中含有的物质是( )
| A. | CuO | B. | Cu | C. | Fe | D. | Cu和Fe |
10.体操运动员在完成单杠、吊环项目时常用“镁粉”搓手,以起到防滑效果.某种“镁粉”中可能含有Mg、MgO、Mg(OH)2、MgCO3中的一种或两种固体,实验小组对其成分展开了探究.
已知:MgO+2HCl═MgCl2+H2O
MgCO3+2HCl═MgCl2+H2O+CO2↑
(1)探究“镁粉”中是否含有Mg和MgCO3
①取少量样品,如图1所示进行实验.观察到a试管中有气泡产生,b试管中产生的现象是澄清石灰水变浑浊.则证明“镁粉”中一定含有MgCO3.
②为证明“镁粉”中是否含有Mg,小明将燃着的木条放在图中b试管口上方,木条熄灭.但同学们指出,该实验不能达成实验目的,需要将图中的澄清石灰水替换成氢氧化钠浓溶液.小明按照修改后的实验方案重复上述实验,观察到b试管口无明显现象,证明“镁粉”中不含Mg.
(2)探究“镁粉”中是否还含有MgO及Mg(OH)2
【实验过程】
Ⅰ.用MgO、Mg(OH)2和MgCO3三种固体分别做性质实验.分别取0.5 g三种固体粉末,每次取样方法如图2所示:
逐滴加入相同溶质质量分数的稀盐酸直至粉末恰好消失.在下表中记录消耗的同浓度稀盐酸的体积(以下体积均在同一条件下测定,且保留到小数点后1位)
Mg(OH)2与盐酸发生中和反应的化学方程式为Mg(OH)2+2HCl═MgCl2+2H2O.
Ⅱ.取“镁粉”样品0.5g,加入上述稀盐酸至粉末恰好溶解.此时消耗稀盐酸的体积约为5.3mL.
【实验分析及结论】
“镁粉”不只含有MgCO3.理由是0.5gMgCO3消耗的盐酸体积与0.5g“镁粉”消耗的盐酸体积不相等
【实验反思】
为确定“镁粉”的具体成分,同学们认为还需要补充如下实验:分别取0.5g“镁粉”和0.5gMgCO3,加入足量稀盐酸,测定生成的气体体积分别为119mL和140mL.由此可知“镁粉”中含有MgCO3的质量分数为85%,“镁粉”中除MgCO3外的另一种物质为Mg(OH)2.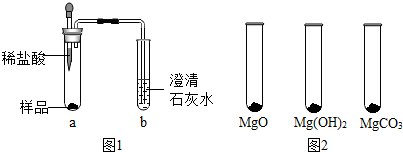
已知:MgO+2HCl═MgCl2+H2O
MgCO3+2HCl═MgCl2+H2O+CO2↑
(1)探究“镁粉”中是否含有Mg和MgCO3
①取少量样品,如图1所示进行实验.观察到a试管中有气泡产生,b试管中产生的现象是澄清石灰水变浑浊.则证明“镁粉”中一定含有MgCO3.
②为证明“镁粉”中是否含有Mg,小明将燃着的木条放在图中b试管口上方,木条熄灭.但同学们指出,该实验不能达成实验目的,需要将图中的澄清石灰水替换成氢氧化钠浓溶液.小明按照修改后的实验方案重复上述实验,观察到b试管口无明显现象,证明“镁粉”中不含Mg.
(2)探究“镁粉”中是否还含有MgO及Mg(OH)2
【实验过程】
Ⅰ.用MgO、Mg(OH)2和MgCO3三种固体分别做性质实验.分别取0.5 g三种固体粉末,每次取样方法如图2所示:
逐滴加入相同溶质质量分数的稀盐酸直至粉末恰好消失.在下表中记录消耗的同浓度稀盐酸的体积(以下体积均在同一条件下测定,且保留到小数点后1位)
| MgO | Mg(OH)2 | MgCO3 | |
| 消耗稀盐酸的体积/mL | 10.4 | 7.2 | 5.0 |
Ⅱ.取“镁粉”样品0.5g,加入上述稀盐酸至粉末恰好溶解.此时消耗稀盐酸的体积约为5.3mL.
【实验分析及结论】
“镁粉”不只含有MgCO3.理由是0.5gMgCO3消耗的盐酸体积与0.5g“镁粉”消耗的盐酸体积不相等
【实验反思】
为确定“镁粉”的具体成分,同学们认为还需要补充如下实验:分别取0.5g“镁粉”和0.5gMgCO3,加入足量稀盐酸,测定生成的气体体积分别为119mL和140mL.由此可知“镁粉”中含有MgCO3的质量分数为85%,“镁粉”中除MgCO3外的另一种物质为Mg(OH)2.

8. 甲为初中化学常见物质,请根据下列叙述回答问题.
甲为初中化学常见物质,请根据下列叙述回答问题.
(1)若甲可以用于灭火,将甲通入紫色石蕊试液中,观察到试液变红色,发生反应的化学方程式为CO2+H2O=H2CO3.
(2)若甲是一种红色固体氧化物,将甲放入过量的稀盐酸中,观察到固体消失,无色溶液变为黄色.反应后所得溶液的溶质为FeCl3、HCl.
(3)若甲含有4种元素且能与稀盐酸反应产生气泡.向甲的溶液中加入过量氢氧化钠溶液,发生反应生成乙和水,但无明显现象;向反应后的溶液中逐滴滴加稀盐酸,一段时间后产生气泡.甲与氢氧化钠溶液的反应方程式为NaHCO3+NaOH=Na2CO3+H2O.
(4)若一定量的甲与乙在一定条件下发生反应,下列情况与图象的对应关系正确的是C (填序号).
0 165529 165537 165543 165547 165553 165555 165559 165565 165567 165573 165579 165583 165585 165589 165595 165597 165603 165607 165609 165613 165615 165619 165621 165623 165624 165625 165627 165628 165629 165631 165633 165637 165639 165643 165645 165649 165655 165657 165663 165667 165669 165673 165679 165685 165687 165693 165697 165699 165705 165709 165715 165723 211419
 甲为初中化学常见物质,请根据下列叙述回答问题.
甲为初中化学常见物质,请根据下列叙述回答问题.(1)若甲可以用于灭火,将甲通入紫色石蕊试液中,观察到试液变红色,发生反应的化学方程式为CO2+H2O=H2CO3.
(2)若甲是一种红色固体氧化物,将甲放入过量的稀盐酸中,观察到固体消失,无色溶液变为黄色.反应后所得溶液的溶质为FeCl3、HCl.
(3)若甲含有4种元素且能与稀盐酸反应产生气泡.向甲的溶液中加入过量氢氧化钠溶液,发生反应生成乙和水,但无明显现象;向反应后的溶液中逐滴滴加稀盐酸,一段时间后产生气泡.甲与氢氧化钠溶液的反应方程式为NaHCO3+NaOH=Na2CO3+H2O.
(4)若一定量的甲与乙在一定条件下发生反应,下列情况与图象的对应关系正确的是C (填序号).
| 甲 | 乙 | y轴含义 | |
| A | 生石灰 | 水 | 固体质量 |
| B | 铜锌合金粉末 | 硫酸铜溶液 | 溶液质量 |
| C | 工业炼铁的尾气 | 氢氧化钠溶液 | 气体质量 |
| D | 密闭容器中的空气 | 红磷 | 反应过程中容器内压强 |

 某化学兴趣小组用如图所示装置研究以下两个问题.
某化学兴趣小组用如图所示装置研究以下两个问题. 水和溶液与人类生存和发展密切相关.
水和溶液与人类生存和发展密切相关.