12.科学家发明了一种在厌氧微生物作用下处理水中有机物(以C6H10O5为例)的新技术,其原理可表示为:2C6H10O5+2O2=7CO2+5X,关于物质X,下列说法正确的是( )
| A. | 该物质由碳、氢、氧三种元素组成 | B. | 该物质的化学式为CH4O | ||
| C. | 该物质中碳、氢元素的质量比为1:4 | D. | 该物质中氢元素的质量分数是25% |
11.下列关于分子、原子的叙述中,不正确的是( )
| A. | 分子由原子构成 | B. | 分子能保持物质的性质 | ||
| C. | 原子由原子核和电子构成 | D. | 原子得失电子可以转化为离子 |
8.下列有关说法中错误的是( )
| A. | 干冰、冰既是纯净物又是化合物. | |
| B. | 分子、原子都是保持物质化学性质的粒子.分子质量不一定大于原子质量. | |
| C. | 纯碱、烧碱溶液都显碱性,都能使酚酞变红,它们属于同类物质 | |
| D. | CO2、CH4、O3都是能造成温室效应的物质 |
7.下列说法正确的是( )
| A. | 煤炉火上放一盆水,就能防止一氧化碳中毒 | |
| B. | 用氢氧化钠固体来除去二氧化碳中的水蒸气 | |
| C. | 发生火灾时,应用湿毛巾捂住口鼻,匍匐前进 | |
| D. | 铝合金灯柱属于合成材料 |
5.下列图示实验操作中,正确的是( )
| A. |  检验二氧化碳 | B. |  将氯化钠倒入 量筒中配制溶液 | ||
| C. |  研磨闻气味鉴别铵态氮肥 | D. |  向试管中 滴加液体 |
4.下列现象能用物理变化解释的是( )
0 164988 164996 165002 165006 165012 165014 165018 165024 165026 165032 165038 165042 165044 165048 165054 165056 165062 165066 165068 165072 165074 165078 165080 165082 165083 165084 165086 165087 165088 165090 165092 165096 165098 165102 165104 165108 165114 165116 165122 165126 165128 165132 165138 165144 165146 165152 165156 165158 165164 165168 165174 165182 211419
| A. | 水壶烧水出现水垢 | B. | 冬季室内窗户玻璃出现水雾 | ||
| C. | 牛奶变酸 | D. | 石墨在一定条件下转化为金刚石 |
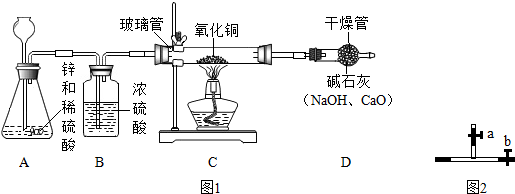
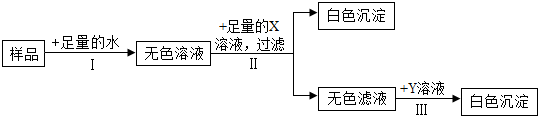
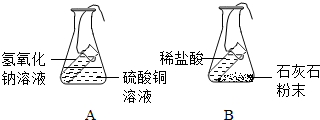 小明为了探究质量守恒定律,设计了A、B两个实验装置(如图所示).
小明为了探究质量守恒定律,设计了A、B两个实验装置(如图所示). F-.
F-.
 B.
B. C.
C.
 B.
B. C.
C. 的个数比是2:1:2.
的个数比是2:1:2.