9.氮化硅是一种新型陶瓷材料,在高温下的氮气流中由石英与焦炭反应制得:3SiO2+6C+2N2═□+6CO.则氮化硅化学式为( )
| A. | SiN | B. | NSi | C. | Si3N4 | D. | N4Si3 |
8.从防火、灭火、自救等安全知识判断,下列做法错误的是( )
| A. |  用明火检验燃气是否泄漏 | B. |  炒菜时油锅着火用锅盖盖灭 | ||
| C. |  室内着火时不急于打开门窗 | D. |  发生火灾逃生时用湿毛巾捂住口鼻 |
7.2015年“世界水日”、“中国水周”的宣传主题为“节约水资源,保障水安全”.下列有关水的认识中错误的是( )
0 164019 164027 164033 164037 164043 164045 164049 164055 164057 164063 164069 164073 164075 164079 164085 164087 164093 164097 164099 164103 164105 164109 164111 164113 164114 164115 164117 164118 164119 164121 164123 164127 164129 164133 164135 164139 164145 164147 164153 164157 164159 164163 164169 164175 164177 164183 164187 164189 164195 164199 164205 164213 211419
| A. | 大量使用农药、化肥,不会造成水体污染 | |
| B. | 可用肥皂水来区分硬水和软水 | |
| C. | 明矾可促进水中悬浮杂质的沉降 | |
| D. | 随意丢弃废电池易造成水土重金属污染 |
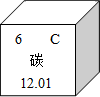 B.碳原子核内质子数为6
B.碳原子核内质子数为6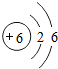 D.碳的相对原子质量为12.01
D.碳的相对原子质量为12.01

 多角度认识物质,能帮助我们更全面了解物质世界.以氧气和二氧化碳为例,回答下列问题:
多角度认识物质,能帮助我们更全面了解物质世界.以氧气和二氧化碳为例,回答下列问题: