3.下列图示的实验操作中,正确的是( )
| A. |  | B. |  | C. |  | D. |  |
2.草木灰的主要成分是碳酸钾(K2CO3),下列关于草木灰的说法中错误的是( )
| A. | 可作钾肥 | B. | 由三种元素组成 | ||
| C. | K2CO3属于盐类 | D. | 碳元素的化合价是+2价 |
1. 化学服务于生活.如表是生活中常用物质溶液的pH,请用化学符号填空:
化学服务于生活.如表是生活中常用物质溶液的pH,请用化学符号填空:
(1)可用于制“叶脉书签”的碱:NaOH(填化学式).
(2)当你被蚊虫叮咬(释放一种酸性物质)后,为减轻疼痛,可在叮咬处涂NaHCO3(填化学式);
(3)酸、碱、盐溶液中发生的反应实质是溶液中的离子反应.酸溶液有相似的性质因为溶液中有共同的H+(填离子符号);碱溶液有相似的性质是溶液中OH-(填离子符号)表现出来的性质
(4)从微观角度认识物质及其变化有助于了解物质的组成及其变化的本质.如图表示氢氧化钠溶液与盐酸反应的微观过程,该反应的本质是H+和OH-结合生成水.请写出一个与上述反应本质相同的化学方程式:H2SO4+2KOH═K2SO4+2H2O.
 化学服务于生活.如表是生活中常用物质溶液的pH,请用化学符号填空:
化学服务于生活.如表是生活中常用物质溶液的pH,请用化学符号填空:| 序号 | A | B | C | D | E |
| 名称 | 食醋 | 白酒 | 白糖水 | 烧碱 | 小苏打溶液 |
| 溶液pH | 3 | 7 | 7 | 11 | 8 |
(2)当你被蚊虫叮咬(释放一种酸性物质)后,为减轻疼痛,可在叮咬处涂NaHCO3(填化学式);
(3)酸、碱、盐溶液中发生的反应实质是溶液中的离子反应.酸溶液有相似的性质因为溶液中有共同的H+(填离子符号);碱溶液有相似的性质是溶液中OH-(填离子符号)表现出来的性质
(4)从微观角度认识物质及其变化有助于了解物质的组成及其变化的本质.如图表示氢氧化钠溶液与盐酸反应的微观过程,该反应的本质是H+和OH-结合生成水.请写出一个与上述反应本质相同的化学方程式:H2SO4+2KOH═K2SO4+2H2O.
20.如表是Ca(OH)2和NaOH的溶解度数据.请回答下列问题:
(1)依据表中数据,溶解度曲线随温度的升高而降低的是Ca(OH)2.
(2)20℃时,NaOH的溶解度为91g.
(3)要想把一瓶接近饱和的Ca(OH)2溶液变成饱和溶液,具体的措施有:①加入氢氧化钙,②升高温度,③减低温度,④加入水,⑤蒸发水后再恢复到原温度,⑥加入生石灰.其中正确的是D.
A.②④⑥B.③④C.①③⑤⑥D.①②⑤⑥
(4)现将20℃时Ca(OH)2的饱和溶液甲溶液降温至0℃得到乙溶液,则两种溶液中溶质的质量分数相比,乙=(填“>”“<”或“=”)甲.
(5)现有60℃时含Ca(OH)2和NaOH两种溶质的饱和溶液,若要得到较纯净的NaOH晶体,应采取的物理方法是降温结晶并过滤.
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度/g | Ca(OH)2 | 0.19 | 0.17 | 0.14 | 0.12 | 0.09 | 0.08 |
| NaOH | 31 | 91 | 111 | 129 | 313 | 336 | |
(2)20℃时,NaOH的溶解度为91g.
(3)要想把一瓶接近饱和的Ca(OH)2溶液变成饱和溶液,具体的措施有:①加入氢氧化钙,②升高温度,③减低温度,④加入水,⑤蒸发水后再恢复到原温度,⑥加入生石灰.其中正确的是D.
A.②④⑥B.③④C.①③⑤⑥D.①②⑤⑥
(4)现将20℃时Ca(OH)2的饱和溶液甲溶液降温至0℃得到乙溶液,则两种溶液中溶质的质量分数相比,乙=(填“>”“<”或“=”)甲.
(5)现有60℃时含Ca(OH)2和NaOH两种溶质的饱和溶液,若要得到较纯净的NaOH晶体,应采取的物理方法是降温结晶并过滤.
19.FeCl3溶液腐蚀铜、铁的反应分别为:Cu+2FeCl3=2FeCl2+CuCl2、Fe+2FeCl3=3FeCl2.从腐蚀过镀铜器件的废液中回收铜,并重新制得FeCl3的流程如下:

下列说法不正确的是( )

下列说法不正确的是( )
| A. | 步骤②中发生化合反应、置换反应和复分解反应 | |
| B. | “滤液1”中一定含FeCl2,一定不含CuCl2 | |
| C. | 步骤④反应为:2M+2FeCl2+H2O2=2FeCl3+2H2O,M是HCl | |
| D. | 若滤渣也为m1g,则废液中FeCl3与CuCl2的质量比为65:56 |
18.分类是学习化学的方法之一,下列物质是按单质、碱、混合物的顺序排列的是( )
| A. | 氧气、纯碱、空气 | B. | 氢气、硫酸、碱式碳酸铜 | ||
| C. | 水、烧碱、生铁 | D. | 金刚石、熟石灰、石油 |
17.下列归类错误的是( )
| 选项 | 归类 | 物质(或元素) |
| A | 常见合金 | 黄铜、硬铝、青铜 |
| B | 常见的干燥剂 | 浓硫酸、生石灰、碱石灰 |
| C | 常见复合材料 | 钢筋混凝土、聚乙烯塑料、玻璃钢 |
| D | 人体中常见微量元素 | 碘、锌、硒、铁等 |
| A. | A | B. | B | C. | C | D. | D |
16.碳在空气中燃烧可以生成CO或CO2.那么,氢气中空气中燃烧除生成水以外,能不能生成其他产物?某研究小组进行了如下探究:
【提出猜想】氢气在空气中燃烧可能生成过氧化氢
【查阅资料】①过氧化氢能使紫色酸性KMnO4溶液褪色;②锌粒与稀H2SO4反应制取氢气可能混有使酸性高锰酸钾溶液褪色的物质.
【设计并完成实验】小明设计了下图所示三套实验装置,点燃氢气并收集液体燃烧物.
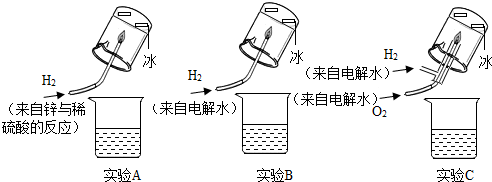
小亮取4只试管,分别加入5滴酸性KMnO4溶液,再加入小明收集的液体产物和蒸馏水,测定恰好使紫色退去所需要的液体体积.
【得出结论】
(1)用锌与稀H2SO4反应制取氢气的化学方程式是Zn+H2SO4=ZnSO4+H2↑.
(2)实验④的实验目的是对照实验.
(3)由实验①、②、③的现象可知,氢气燃烧有(填“有”或“无”)过氧化氢生成.
(4)对比实验①和②可知,用锌粒与稀H2SO4反应制得氢气不纯(填“纯”或“不纯”).
(5)实验③比实验②更接近事实,因为它可排除空气中其他成分的干扰.
【反思与评价】
“用锌和稀H2SO4反应制氢气”与“电解水制氢气.氧气”,分别进行试验①和试验③,各自的优、缺点是:前者易于操作;后者反应物、生成物纯净(氢气、氧气和水)后者原子利用率高于前者(后者电解水产生的氢气和氧气恰好完全反应,而前者制氢气时产物还有硫酸锌,点燃时消耗空气中氧气).
【提出猜想】氢气在空气中燃烧可能生成过氧化氢
【查阅资料】①过氧化氢能使紫色酸性KMnO4溶液褪色;②锌粒与稀H2SO4反应制取氢气可能混有使酸性高锰酸钾溶液褪色的物质.
【设计并完成实验】小明设计了下图所示三套实验装置,点燃氢气并收集液体燃烧物.

小亮取4只试管,分别加入5滴酸性KMnO4溶液,再加入小明收集的液体产物和蒸馏水,测定恰好使紫色退去所需要的液体体积.
| 实验序号 | 加入液体 | 实验现象 |
| ① | 实验A 的收集液4.0mL | 褪色 |
| ② | 实验B 的收集液5.5mL | 褪色 |
| ③ | 实验C的收集液10.0mL | 不褪色 |
| ④ | 蒸馏水10.0mL | 不褪色 |
(1)用锌与稀H2SO4反应制取氢气的化学方程式是Zn+H2SO4=ZnSO4+H2↑.
(2)实验④的实验目的是对照实验.
(3)由实验①、②、③的现象可知,氢气燃烧有(填“有”或“无”)过氧化氢生成.
(4)对比实验①和②可知,用锌粒与稀H2SO4反应制得氢气不纯(填“纯”或“不纯”).
(5)实验③比实验②更接近事实,因为它可排除空气中其他成分的干扰.
【反思与评价】
“用锌和稀H2SO4反应制氢气”与“电解水制氢气.氧气”,分别进行试验①和试验③,各自的优、缺点是:前者易于操作;后者反应物、生成物纯净(氢气、氧气和水)后者原子利用率高于前者(后者电解水产生的氢气和氧气恰好完全反应,而前者制氢气时产物还有硫酸锌,点燃时消耗空气中氧气).
15.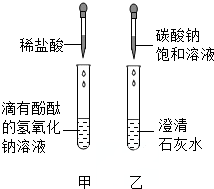 同学们在学碱的化学性质时,做了如图所示的甲、乙两个实验.
同学们在学碱的化学性质时,做了如图所示的甲、乙两个实验.
(1)写出甲实验的化学反应方程式HCl+NaOH=NaCl+H2O.
(2)实验结束后,甲、乙两个同学将废液倒入实验室的废液缸中,结果发现废液浑浊并呈红色,于是他们产生了疑问.
【提出问题】废液中含有哪些物质?
【交流讨论】①一定含有的物质:碳酸钙、指示剂、NaCl和水.
②还含有能使废液呈碱性的物质.能使废液呈碱性的物质是什么?同学们有如下猜想.
小刚认为:只有碳酸钠
小红认为:只有氢氧化钙
小林认为:是氢氧化钠和碳酸钠
你认为还可能是NaOH.(写一种猜想)
【设计实验】小芳想用氯化钙溶液来验证小刚、小红、小林的猜想.查阅资料得知氯化钙溶液呈中性,并设计如下实验.请你将小芳的实验设计补充完整.
【反思拓展】在分析化学反应后所得物质的成分时,除了考虑生成物外还需考虑反应物的用量.
0 163764 163772 163778 163782 163788 163790 163794 163800 163802 163808 163814 163818 163820 163824 163830 163832 163838 163842 163844 163848 163850 163854 163856 163858 163859 163860 163862 163863 163864 163866 163868 163872 163874 163878 163880 163884 163890 163892 163898 163902 163904 163908 163914 163920 163922 163928 163932 163934 163940 163944 163950 163958 211419
 同学们在学碱的化学性质时,做了如图所示的甲、乙两个实验.
同学们在学碱的化学性质时,做了如图所示的甲、乙两个实验.(1)写出甲实验的化学反应方程式HCl+NaOH=NaCl+H2O.
(2)实验结束后,甲、乙两个同学将废液倒入实验室的废液缸中,结果发现废液浑浊并呈红色,于是他们产生了疑问.
【提出问题】废液中含有哪些物质?
【交流讨论】①一定含有的物质:碳酸钙、指示剂、NaCl和水.
②还含有能使废液呈碱性的物质.能使废液呈碱性的物质是什么?同学们有如下猜想.
小刚认为:只有碳酸钠
小红认为:只有氢氧化钙
小林认为:是氢氧化钠和碳酸钠
你认为还可能是NaOH.(写一种猜想)
【设计实验】小芳想用氯化钙溶液来验证小刚、小红、小林的猜想.查阅资料得知氯化钙溶液呈中性,并设计如下实验.请你将小芳的实验设计补充完整.
| 实验内容 | 预计现象 | 预计结论 |
| 取少量废液缸中上层清液于试管 中,加入过量氯化钙溶液,静置. | ①有白色沉淀,溶液呈红色. | 小林的猜想正确. |
| ②产生白色沉淀、溶液为无色. | 小刚的猜想正确. | |
| ③无白色沉淀,溶液呈红色. | 小红的猜想正确. |
