9.下列叙述与对应的化学方程式、所属基本反应类型都正确的是( )
| A. | 高炉炼铁的主要反应2Fe2O3+3C$\frac{\underline{\;高温\;}}{\;}$3CO2↑+4Fe置换反应 | |
| B. | 实猃室用过氧化氢制取氧气2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑分解反应 | |
| C. | 用氢氧化钠洗涤石油产品中的硫酸2NaOH+H2SO4=Na2SO4+H2O中和反应 | |
| D. | 鉴别黄铜与18K黄金Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$CuO化合反应 |
8.人体健康与化学关系密切,下列叙述错误的是( )
| A. | 纤维素是构成植物细胞的基础物质,不能被人体消化,蔬菜和粗粮等含纤维素较多 | |
| B. | 青少年缺锌会引起生长迟缓,发育不良,可适当食用海产品、奶类、小米等食物 | |
| C. | 为减轻蚊虫叮咬后的痛痒感,可涂抹牙膏、肥皂水等 | |
| D. | 维生素有20多种,多数在人体内不能合成,缺乏维生素C,会引起夜盲症 |
7.下列物质的用途错误的是( )
| A. |  烧碱用于制披璃 | B. |  稀有气体制成强照明灯 | ||
| C. |  硫酸用于制农药 | D. |  氯化钠溶液用于选种 |
6.下列做法正确的是( )
| A. | 用活性炭净水器能除去水中的可溶性钙、镁化合物 | |
| B. | 不慎碰倒酒精灯,酒精在桌面上燃烧,使用水基型灭火器灭火 | |
| C. | 为防止菜刀生锈在表面镀铜 | |
| D. | 为防止玉米、薯干发生霉变,应将其储存在干燥通风处 |
5.下列实验操作正确的是( )
| A. |  量取8mL液体 | B. |  由试管底部套上试管夹 | ||
| C. |  测定空气中氧气的含量 | D. |  除去CO中的CO2 |
4.下列过程中未发生化学变化的是( )
| A. |  明矾净水 | B. |  铁钉部分浸没在食盐水中 | ||
| C. |  探究燃烧的条件 | D. |  甲醛溶液浸泡动物标本 |
3. “冰城制造”助国产大飞机C919 一飞冲天,中航工业哈飞作为我国首架自主研制的大型客机C919机体结构的制造商主要承担了 4个大部件工作包的制造.下列有关叙述错误的是( )
“冰城制造”助国产大飞机C919 一飞冲天,中航工业哈飞作为我国首架自主研制的大型客机C919机体结构的制造商主要承担了 4个大部件工作包的制造.下列有关叙述错误的是( )
 “冰城制造”助国产大飞机C919 一飞冲天,中航工业哈飞作为我国首架自主研制的大型客机C919机体结构的制造商主要承担了 4个大部件工作包的制造.下列有关叙述错误的是( )
“冰城制造”助国产大飞机C919 一飞冲天,中航工业哈飞作为我国首架自主研制的大型客机C919机体结构的制造商主要承担了 4个大部件工作包的制造.下列有关叙述错误的是( )| A. | 参与国产大飞机制造,有效提升了龙江航空产业制造能力 | |
| B. | 制造客机使用的复合材料主要有机破璃、碳纤维复合材料等 | |
| C. | 制造客机使用的硬铝的主要成分是铝、铜、镁、硅 | |
| D. | 客机使用的燃料航空煤油是石油炼制的产品 |
2.小明为了测定某石灰石中碳酸钙的质量分数,用如图装置进行如下实验: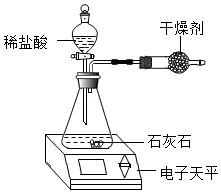
①取研碎后的石灰石2.5克,倒入气密性良好的锥形瓶中,然后在分液漏斗中加入适量的稀盐酸,置于电子天平上测出装置总质量.
②打开活塞,滴入足量稀盐酸后关闭活塞,待气泡不再冒出时,测出反应后装置总质量.
③整理相关数据如下表,计算出石灰石中碳酸钙的质量分数.
(1)该实验中,对装置中的固态干燥剂的性质有何要求?能吸收水不能吸收二氧化碳.
(2)结合表中数据,计算该石灰石中碳酸钙的质量分数.(CaCO3+2HCl=CaCl2+H2O+CO2↑,石灰石中的其它成分不与盐酸反应)
(3)实验后小明认真反思觉得该实验测得的石灰石中碳酸钙的质量分数比实际值会偏小(填“偏大”、“偏小”或“不变”),理由是反应后有部分二氧化碳残留在锥形瓶中使测量得到的二氧化碳的质量变小,故计算得到的碳酸
钙的质量也变小.
0 158082 158090 158096 158100 158106 158108 158112 158118 158120 158126 158132 158136 158138 158142 158148 158150 158156 158160 158162 158166 158168 158172 158174 158176 158177 158178 158180 158181 158182 158184 158186 158190 158192 158196 158198 158202 158208 158210 158216 158220 158222 158226 158232 158238 158240 158246 158250 158252 158258 158262 158268 158276 211419

①取研碎后的石灰石2.5克,倒入气密性良好的锥形瓶中,然后在分液漏斗中加入适量的稀盐酸,置于电子天平上测出装置总质量.
②打开活塞,滴入足量稀盐酸后关闭活塞,待气泡不再冒出时,测出反应后装置总质量.
③整理相关数据如下表,计算出石灰石中碳酸钙的质量分数.
| 反应前总质量(克) | 275.58 |
| 反应后总质量(克) | 274.70 |
| 反应前后质量差(克) | 0.88 |
(2)结合表中数据,计算该石灰石中碳酸钙的质量分数.(CaCO3+2HCl=CaCl2+H2O+CO2↑,石灰石中的其它成分不与盐酸反应)
(3)实验后小明认真反思觉得该实验测得的石灰石中碳酸钙的质量分数比实际值会偏小(填“偏大”、“偏小”或“不变”),理由是反应后有部分二氧化碳残留在锥形瓶中使测量得到的二氧化碳的质量变小,故计算得到的碳酸
钙的质量也变小.
 如图是小明在实验室里用一氧化碳还原氧化铁来模拟高炉炼铁反应,其原理可用化学方程式表示为Fe2O3+3CO $\frac{\underline{\;高温\;}}{\;}$Fe+3CO2.
如图是小明在实验室里用一氧化碳还原氧化铁来模拟高炉炼铁反应,其原理可用化学方程式表示为Fe2O3+3CO $\frac{\underline{\;高温\;}}{\;}$Fe+3CO2.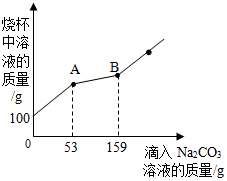 在一烧杯中盛有BaCl2和HCl的混合溶液,向其中逐渐滴加溶质质量分数为10%的Na2CO3溶液,混合溶液的质量与所滴入Na2CO3溶液的质量关系曲线如图所示,请根据题意问答问题:
在一烧杯中盛有BaCl2和HCl的混合溶液,向其中逐渐滴加溶质质量分数为10%的Na2CO3溶液,混合溶液的质量与所滴入Na2CO3溶液的质量关系曲线如图所示,请根据题意问答问题: