2.有20gFe2O3和CuO的混合物,进行如下实验:把混合物全部加入到l00g的硫酸溶液中,完全溶解.然后滴加150gl6%的NaOH溶液,恰好完全沉淀.则所用硫酸溶液溶质的质量分数为( )
| A. | 无法计算 | B. | 29.4% | C. | 24% | D. | 36.8% |
20.CO2是重要的资源,以其为原料可获得下列四种物质.下列说法错误的是( )


| A. | 反应①维持自然界的碳氧平衡,将太阳能转化为化学能 | |
| B. | 反应②的产品为有机高分子化合物,可有利于缓解“白色污染” | |
| C. | 反应③是化合反应,产品属氮肥 | |
| D. | 反应④获得产品后的剩余液中,溶质有NH4Cl和NaHCO3 |
19. 如图是甲、乙、丙三种固体物质的溶解度曲线,下列说法不正确的是( )
如图是甲、乙、丙三种固体物质的溶解度曲线,下列说法不正确的是( )
 如图是甲、乙、丙三种固体物质的溶解度曲线,下列说法不正确的是( )
如图是甲、乙、丙三种固体物质的溶解度曲线,下列说法不正确的是( )| A. | 将丙物质饱和溶液变为不饱和溶液,可采用降温方法 | |
| B. | 70℃时,分别用100g水配制甲、乙的饱和溶液,再降温到20℃,析出无水晶体的质量:甲>乙 | |
| C. | 50℃时,将等质量的甲、乙、丙三种固体分别配制成饱和溶液,需加水质量最多的是丙 | |
| D. | 将40℃时甲、乙、丙的饱和溶液分别升温至60℃,所得溶液的溶质质量分数由大到小的顺序是:乙>甲=丙 |
18.鉴别下列各组物质,所用两组试剂有错误的是( )
| 选项 | 待鉴别物质 | 鉴别试剂1 | 鉴别试剂2 |
| A | 硝酸铵固体和氢氧化钠固体 | 水 | 熟石灰 |
| B | 盐酸和稀硫酸 | 氯化钡溶液 | 石灰石 |
| C | 氯化钠溶液和碳酸钠溶液 | 盐酸 | 酚酞 |
| D | 氧气、二氧化碳、氮气 | 澄清石灰水 | 燃着的木条 |
| A. | A | B. | B | C. | C | D. | D |
17.下列各组离子能在指定溶液中大量共存的一组是( )
| A. | 在pH=l 的溶液中:Na+、NO3-、CO32- | |
| B. | 能使石蕊变红的溶液中:K+、NH4+、Cl- | |
| C. | 在硫酸铜溶液中:Ba2+、Zn2+、CO32- | |
| D. | 在碳酸氢铵溶液中:K+、OH-、NO3- |
16.为了测定某陨石中铁的含量,某化学兴趣小组的同学进行了以下实验:取四份相同质量的样品分别放入等质量的烧杯中,然后分别加入稀硫酸,充分反应后用天平称量,(杂质不与稀硫酸反应产生气体)几次试验数据如下,请回答下列问题并计算:
(1)在第1次实验结束后,反应物硫酸完全反应完了.
(2)50.0g样品与足量稀硫酸反应最多能生成气体0.5g.
(3)计算陨石中铁的质量分数(写出具体计算过程).
0 158057 158065 158071 158075 158081 158083 158087 158093 158095 158101 158107 158111 158113 158117 158123 158125 158131 158135 158137 158141 158143 158147 158149 158151 158152 158153 158155 158156 158157 158159 158161 158165 158167 158171 158173 158177 158183 158185 158191 158195 158197 158201 158207 158213 158215 158221 158225 158227 158233 158237 158243 158251 211419
| 试验次序 | 第1次 | 第2次 | 第3次 | 第4次 |
| 所取样品的质量/g | 50.0 | 50.0 | 50.0 | 50.0 |
| 加入稀硫酸的质量/g | 20.0 | 40.0 | 60.0 | 80.0 |
| 生成气体的质量/g | 0.2 | 0.4 | 0.5 | 0.5 |
(2)50.0g样品与足量稀硫酸反应最多能生成气体0.5g.
(3)计算陨石中铁的质量分数(写出具体计算过程).
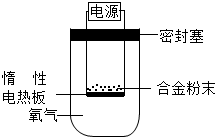 镁是一种活泼金属,除了能与氧气反应,还可以与氮气、二氧化碳等反应.为测定镁铝合金(不含其他元素)中镁的质量分数,称量ag镁铝合金粉末,放在如图所示装置的惰性电热板上,通电使其充分灼烧.下列关于该实验的说法正确的是( )
镁是一种活泼金属,除了能与氧气反应,还可以与氮气、二氧化碳等反应.为测定镁铝合金(不含其他元素)中镁的质量分数,称量ag镁铝合金粉末,放在如图所示装置的惰性电热板上,通电使其充分灼烧.下列关于该实验的说法正确的是( ) 如图为硝酸钾和氯化钾的溶解度曲线,请据图完成下列问题:
如图为硝酸钾和氯化钾的溶解度曲线,请据图完成下列问题: