1.下列关于物质组成结构的说法正确的是( )
| A. | 原子核都是由质子和中子构成 | B. | 原子团在化学变化中不可分 | ||
| C. | 溶液一定是均一、稳定的混合物 | D. | 氧化物就是含有氧元素的化合物 |
14.不规范的实验操作可能会影响化学实验的结果.下列实验操作中正确的是( )
| A. | 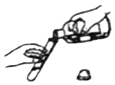 向试管中加入液体 | B. |  用胶头滴管吸取液体 | ||
| C. | 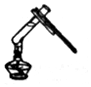 给盛有液体的试管加热 | D. | 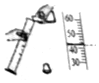 量取液体的值 |
13.将20gCaCO3隔绝空气高温煅烧一段时间后停止,剩余固体中钙元素的质量分数为50%,则整个过程中产生二氧化碳的质量为( )
| A. | 2.2g | B. | 4g | C. | 4.4g | D. | 8g |
10.在CuO和Fe的混合物中加入一定量的稀硫酸,微热,待反应停止后过滤,滤出不溶物后再往滤液里加入一枚铁钉,若铁钉表面有气泡产生.则错误的叙述是( )
| A. | 不溶物中一定有铜 | |
| B. | 不溶物可能全部是铁 | |
| C. | 滤液是硫酸亚铁溶液 | |
| D. | 滤液是硫酸铜和硫酸亚铁的混合溶液 |
8.实验室制取氧气(装置从图中选择)

(1)用高锰酸钾制取氧气时,试管口应放一团棉花,目的是防止加热时高锰酸钾粉末进入导管,用E装置收集氧气的最佳时间是导管口气泡连续、均匀冒出时,实验完毕后先将导管从水槽中移出,再熄灭酒精灯,原因是防止水倒吸入热的试管,引起试管炸裂.
(2)用A装置制取氧气需加入黑色固体二氧化锰,所起的作用是催化作用.
(3)工业上制取氧气的方法是分离液态空气,该方法属于物理变化.

| 药品的化学式及色、态 | KClO3(白色固体)、MnO2(黑色固体) | KMnO4(暗紫色固体) | H2O2(无色液体)、MnO2(黑色固体) | |
| 原理(化学方程式) | 2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑ | 2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑ | 2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑ | |
| 装置 | 发生装置 | B | B | A |
| 收集装置 | D(或E) | D(或E) | D(或E) | |
| 操作步骤 | 检查装置气密性,加入药品,固定试管,加热,收集,验满,熄灭酒精灯,洗涤整理(或检查装置气密性,加入药品,固定试管,加热,收集,收集完毕将导管从水中移出,熄灭酒精灯,洗涤仪器) | 检查装置气密性,加入药品,固定试管,加热,收集,验满,熄灭酒精灯,洗涤整理(或检查装置气密性,加入药品,固定试管,加热,收集,收集完毕将导管从水中移出,熄灭酒精灯,洗涤仪器) | 检查装置气密性,加入药品,固定试管,收集,验满,洗涤整理(或检查装置气密性,加入药品,固定试管,加热,收集,收集完毕将导管从水中移出,熄灭酒精灯,洗涤仪器) | |
| 验证方法 | 将带 火星的木条伸入集气瓶中,若木条复燃则是氧气 | 将带 火星的木条伸入集气瓶中,若木条复燃则是氧气 | 将带 火星的木条伸入集气瓶中,若木条复燃则是氧气 | |
| 验满方法 | 将带 火星的木条放于集气瓶口,若木条复燃则满(或瓶口有大气泡冒出则满) | 将带 火星的木条放于集气瓶口,若木条复燃则满(或瓶口有大气泡冒出则满) | 将带 火星的木条放于集气瓶口,若木条复燃则满(或瓶口有大气泡冒出则满) | |
(2)用A装置制取氧气需加入黑色固体二氧化锰,所起的作用是催化作用.
(3)工业上制取氧气的方法是分离液态空气,该方法属于物理变化.
7.下列说法错误的是( )
| A. | 饱和溶液所含溶质的质量一定比不饱和溶液的多 | |
| B. | 铅锑合金的熔点较低,用来做保险丝 | |
| C. | 甲醛有防腐作用,但不能用于食品保鲜 | |
| D. | 钳子、羊角锤和开瓶的起子都是省力杠杆 |
6.鸡蛋壳的主要成分是碳酸钙,为测定鸡蛋壳中的碳酸钙含量,某同学将鸡蛋壳洗净、充分干燥并捣碎,展开了下列探究.
(1)将20ml溶质质量分数为35%的浓盐酸配制成10%的稀盐酸,操作步骤为:
步骤1:计算20ml溶质质量分数为35%的浓盐酸的质量为24g;
(溶质质量分数为35%的浓盐酸的密度ρ为1.2g/ml)
步骤2:计算所需加入水的体积为60ml;
步骤2:根据计算结果,用量筒分别量取所需的水和浓盐酸;
步骤3:先量取水倒入烧杯中,然后量取浓盐酸倒入水中并用玻璃棒搅拌得到稀盐酸.
(2)测得鸡蛋壳、空烧杯的质量后,将16g鸡蛋壳置于烧杯中,将配制的稀盐酸全部加入(盐酸过量),用玻璃棒充分搅拌,使其充分反应,直到不再产生气泡为止(假设鸡蛋壳中的其他物质不与稀盐酸反应).实验数据记录 如表:
①实验中生成二氧化碳的质量为4.4g.
②计算该鸡蛋壳中碳酸钙的质量分数.
0 155397 155405 155411 155415 155421 155423 155427 155433 155435 155441 155447 155451 155453 155457 155463 155465 155471 155475 155477 155481 155483 155487 155489 155491 155492 155493 155495 155496 155497 155499 155501 155505 155507 155511 155513 155517 155523 155525 155531 155535 155537 155541 155547 155553 155555 155561 155565 155567 155573 155577 155583 155591 211419
(1)将20ml溶质质量分数为35%的浓盐酸配制成10%的稀盐酸,操作步骤为:
步骤1:计算20ml溶质质量分数为35%的浓盐酸的质量为24g;
(溶质质量分数为35%的浓盐酸的密度ρ为1.2g/ml)
步骤2:计算所需加入水的体积为60ml;
步骤2:根据计算结果,用量筒分别量取所需的水和浓盐酸;
步骤3:先量取水倒入烧杯中,然后量取浓盐酸倒入水中并用玻璃棒搅拌得到稀盐酸.
(2)测得鸡蛋壳、空烧杯的质量后,将16g鸡蛋壳置于烧杯中,将配制的稀盐酸全部加入(盐酸过量),用玻璃棒充分搅拌,使其充分反应,直到不再产生气泡为止(假设鸡蛋壳中的其他物质不与稀盐酸反应).实验数据记录 如表:
| 鸡蛋壳的质量 | 空烧杯的质量 | 充分反应后,烧杯及内容物的总重量 |
| 16g | 60g | 155.6g |
②计算该鸡蛋壳中碳酸钙的质量分数.