题目内容
11.氢有三种同位素-1H(氕)、2H(氘)、3H(氚),由后两种同位素形成的水分别称为“重水”“超重水”,则这两种“水”的相对分子质量之比为10:11;一个超重水分子含有10个电子.分析 相对分子的质量为组成分子的各原子的相对原子质量之和,并结合重水分子和重水分子的构成等进行分析解答.
解答 解:根据题意:一个重水分子是由两个重氢原子和一个氧原子构成,重氢原子的相对原子质量为2,故重水的相对分子质量为2×2+16=20;
一个超重水分子是由两个超重氢原子和一个氧原子构成,超重氢原子的相对原子质量为3,故超重水的相对分子质量为2×3+16=22;
故二者的相对分子质量之比为:20:22=10:11;
在原子中:核电荷数=质子数=核外电子数,超重氢原子的质子数为1,故重氢原子核外有1个电子,氧原子是8号元素,核电荷数是8,则氧原子核外有8个电子,则一个超重水分子含有的电子数是:2+8=10;
故答案为:10:11;10.
点评 掌握原子中核电荷数=质子数=电子数、相对分子质量的计算方法,及运用所学化学知识综合分析和解决实际问题的能力是正确解答本题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
2.在日常生活中,下列做法错误的是( )
| A. | 把水喷向空中,增加养鱼池中氧气的溶解度 | |
| B. | 用硝酸铵制冰袋给发烧的病人降温 | |
| C. | 用汽油洗去衣服上的油渍 | |
| D. | 被雨水淋湿的自行车要先用干布擦净后才能用带油的布擦 |
9.下列方法可以使硬水软化的是( )
| A. | 过滤 | B. | 吸附 | C. | 蒸馏 | D. | 通入氯气 |
6.将下列日常生活中的调味品加入水中,不能形成溶液的是( )
| A. | 食盐 | B. | 白糖 | C. | 味精 | D. | 花生油 |
7.下列实验能达到目的是( )
| A. | 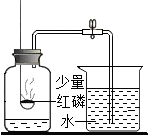 测定空气中氧气含量 | B. | 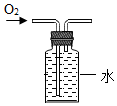 收集氧气 | ||
| C. | 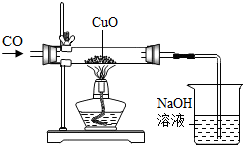 吸收尾气一氧化碳,防止污染空气 | D. | 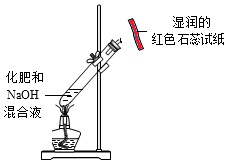 鉴别化肥氯化铵与硝酸钾 |
1.下列实验数据的叙述正确的是( )
| A. | 用10mL量筒量取6.8mL水 | |
| B. | 用托盘天平(精确度:0.1g)称取50g食盐 | |
| C. | 将100g10%的稀盐酸加热蒸发掉50g水,使得稀盐酸溶质质量分数变成20% | |
| D. | 用pH试纸测定某溶液的pH=5.6 |
19.中国科学家屠呦呦和她的团队发现了青蒿素(化学式C15H22O5),挽救了全球数百万人的生命,因而获得诺贝尔生理学或医学奖,下列有关青蒿素的说法正确的是( )
| A. | 青蒿素中碳元素的质量分数最大 | B. | 1个青蒿素分子中含有40个原子 | ||
| C. | 青蒿素是由3种元素组成的混合物 | D. | 青蒿素中碳、氧元素的质量比为3:1 |
6.鸡蛋壳的主要成分是碳酸钙,为测定鸡蛋壳中的碳酸钙含量,某同学将鸡蛋壳洗净、充分干燥并捣碎,展开了下列探究.
(1)将20ml溶质质量分数为35%的浓盐酸配制成10%的稀盐酸,操作步骤为:
步骤1:计算20ml溶质质量分数为35%的浓盐酸的质量为24g;
(溶质质量分数为35%的浓盐酸的密度ρ为1.2g/ml)
步骤2:计算所需加入水的体积为60ml;
步骤2:根据计算结果,用量筒分别量取所需的水和浓盐酸;
步骤3:先量取水倒入烧杯中,然后量取浓盐酸倒入水中并用玻璃棒搅拌得到稀盐酸.
(2)测得鸡蛋壳、空烧杯的质量后,将16g鸡蛋壳置于烧杯中,将配制的稀盐酸全部加入(盐酸过量),用玻璃棒充分搅拌,使其充分反应,直到不再产生气泡为止(假设鸡蛋壳中的其他物质不与稀盐酸反应).实验数据记录 如表:
①实验中生成二氧化碳的质量为4.4g.
②计算该鸡蛋壳中碳酸钙的质量分数.
(1)将20ml溶质质量分数为35%的浓盐酸配制成10%的稀盐酸,操作步骤为:
步骤1:计算20ml溶质质量分数为35%的浓盐酸的质量为24g;
(溶质质量分数为35%的浓盐酸的密度ρ为1.2g/ml)
步骤2:计算所需加入水的体积为60ml;
步骤2:根据计算结果,用量筒分别量取所需的水和浓盐酸;
步骤3:先量取水倒入烧杯中,然后量取浓盐酸倒入水中并用玻璃棒搅拌得到稀盐酸.
(2)测得鸡蛋壳、空烧杯的质量后,将16g鸡蛋壳置于烧杯中,将配制的稀盐酸全部加入(盐酸过量),用玻璃棒充分搅拌,使其充分反应,直到不再产生气泡为止(假设鸡蛋壳中的其他物质不与稀盐酸反应).实验数据记录 如表:
| 鸡蛋壳的质量 | 空烧杯的质量 | 充分反应后,烧杯及内容物的总重量 |
| 16g | 60g | 155.6g |
②计算该鸡蛋壳中碳酸钙的质量分数.